1、选择题 一定条件下用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g) +4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
下列选项正确的是
[? ]
A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
B.反应CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)的焓变为△H3,△H3>△H1
C.若用0.2 mol CH4还原NO2至N2,则反应中放出的热量一定为173.4 kJ
D.若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子的物质的量为3.2 mol
参考答案:A
本题解析:
本题难度:一般
2、简答题 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5?μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl-
浓度/mol?L-1
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
|
根据表中数据判断PM2.5的酸碱性为______,试样的pH=______.
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.
已知:H2?(g)+O2?(g)=H2O;△H=-241.81kJ?mol-1
C?(s)+O2?(g)=CO?(g);△H=-110.51kJ?mol-1
写出焦炭与水蒸气反应的热化学方程式:______.
②洗涤含SO2的烟气.以下物质可作洗涤剂的是______.
a.Ca(OH)2?b.Na2CO3?c.CaCl2?d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g)?2NO?(g);△H>0
若1mol空气含0.8mol?N2和0.2mol?O2,1300℃时在密闭容器内反应达到平衡,测得NO为:8×10-4?mol.计算该温度下的平衡常数:K=______.
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是______.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO?(g)=2C?(s)+O2?(g)
已知该反应的△H>0,简述该设想能否实现的依据:______.
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为______.
参考答案:(1)观察表格中发现NH4+水解显酸性,PM2.5的酸碱性为酸性.试样的pH值根据溶液中电荷守恒计算H+离子浓度为10-4,PH值为4,故答案为:酸性;4;
(2)①已知:①H2 (g)+12O2 (g)=H2O(g);△H=-241.81kJ?mol-1,
②C (s)+12O2 (g)=CO (g);△H=-110.51kJ?mol-1,
利用盖斯定律,将②-①可得C(s)+H2O(g)=CO(g)+H2(g);△H=(-110.51kJ?mol-1)-(-241.81kJ?mol-1)=++13l.3 kJ?mol-1,
故答案为:C(s)+H2O(g)=CO(g)+H2(g);△H=+13l.3?kJ?mol-1;
?②洗涤含SO2的烟气,根据酸性氧化物的性质选a.Ca(OH)2 b.Na2CO3,故答案为:a、b;
(3)①计算平衡常数时,先计算物质的平衡量,N2为0.8mol-4×10-4 mol,O2为0.2mol-4×10-4 mol,带入平衡常数表达式即可,得K=4×10-6,气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移,
故答案为:4×10-6;温度升高,反应速率加快,平衡右移;
②2CO(g)=2C(s)+O2(g),该反应是焓增、熵减的反应.根据G=△H-T?△S,G>0,不能实现,故答案为:该反应是焓增、熵减的反应,任何温度下均不自发进行;
③汽车尾气系统中装置反应的化学方程式为2CO+2NO ?催化剂?.? 2CO2+N2,故答案为:2CO+2NO??催化剂?.??2CO2+N2.
本题解析:
本题难度:一般
3、选择题 已知:
Fe2O3(s)+3/2C(s)== 3/2CO2(g)+2Fe(s);△H=234.1KJ/mol
C(s)+ O2(g)== CO2(g);?△H= -393.5KJ/mol
则4Fe(s)+ 3O2(g)== 2Fe2O3(s)的△H是
[? ]
A.-1648.8KJ/mol
B.-824.4KJ/mol
C.+1648.8KJ/mol
D.-744.7KJ/mol
参考答案:A
本题解析:
本题难度:一般
4、选择题 已知:Fe2O3(s)+C(s)=CO2(g)+2Fe(s),ΔH=+234.1kJ・mol-1
C(s)+O2(g)=CO2(g);ΔH=-393.5kJ・mol-1
则2Fe(s)+ O2(g)=Fe2O3(s)的ΔH是
[? ]
A、-824.4 kJ・mol-1
B、-627.6kJ・mol-1
C、-744.7kJ・mol-1
D、-169.4kJ・mol-1
参考答案:A
本题解析:
本题难度:一般
5、简答题 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)?设计的双液原电池,可以提供稳定的电流.装置如图所示,其中盐桥中装有琼脂-饱和KCl溶液.
回答下列问题:
①电极X的材料和电解质溶液Y分别为______、______;
②盐桥中K+移向______(填A或B);
③银电极发生的电极反应为______.
(2)已知:C(s)+O2(g)=CO2(g)△H1=-396.5kJ?mol-1
H2(g)+1/2O2=H2O(g)△H2=-241.8kJ?mol-1
CO(g)+1/2O2(g)=CO2(g)△H3=-283.0kJ?mol-1
根据盖斯定律写出单质碳和水蒸气生成水煤气的热化学方程式:______.
(3)100mL?1.0mol?L-1盐酸与100mL1.0mol?L-1NaOH溶液在量热计中进行中和反应.测得反应后溶液温度升高了6.8℃,已知稀溶液的比热容为4.2kJ/℃?kg-1,则该中和反应的反应热为______.(小数点后面保留一位有效数字)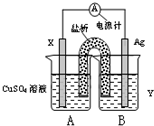
参考答案:(1)①氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)中,活泼的失电子的金属Cu为负极,得电子的阳离子Ag+是电解质中的阳离子,所以电解质可以选择AgNO3溶液;
②原电池反应,B池中Ag+析出,为符合溶液的电中性,盐桥中的钾离子移向B池;
③银电极发生的电极反应为溶液中的银离子得到电子析出银单质,电极反应为:Ag++e-=Ag;
故答案为:Cu、AgNO3溶液;B;Ag++e-=Ag;
(2)①C(s)+O2(g)=CO2(g)△H1=-396.5kJ?mol-1
②H2(g)+1/2O2=H2O(g)△H2=-241.8kJ?mol-1
③CO(g)+1/2O2(g)=CO2(g)△H3=-283.0kJ?mol-1
根据盖斯定律,①-②-③得到:单质碳和水蒸气生成水煤气的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g)△H=128.3 kJ?mol-1
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=128.3 kJ?mol-1;
(3)100mL 1.0mol?L-1盐酸与100mL1.0mol?L-1NaOH溶液在量热计中进行中和反应.生成水为0.1mol,测得反应后溶液温度升高了6.8℃,已知稀溶液的比热容为4.2kJ/°C?kg-1,可以根据计算公式计算得到:Q=-C(T2-T1);稀溶液的密度可以近似为1g/ml,所以Q=-C(T2-T1)=-4.2kJ/°C?kg-1×6.8°C×(200ml×1g/ml×10-3kg/g)=5.71KJ;中和反应生成0.1molH2O,中和反应的反应热是生成1mol水时放出的热量,所以反应的中和热为57.1KJ/mol,
故答案为:57.1 kJ?mol-1.
本题解析:
本题难度:一般