1、简答题 聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n?XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出.其制备原料主要是铝加工行业的废渣--铝灰,它主要含Al2O3、Al,还有SiO2等杂质.聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式为:______;______.
(2)生产过程中B和D的操作名称分别是______和______(B和D均为简单操作).
(3)反应中副产品a是______.
(4)生产过程中可循环使用的物质是______(用化学式表示).
(5)调节pH至4.0~4.5的目的是______.
(6)实验室要测定水处理剂产品中n和x的值.为使测定结果更准确,需得到的晶体较纯净.生产过程C物质可选用______.
A.NaOH? B.Al? C.氨水? D.Al2O3 E.NaAlO2.
参考答案:(1)氧化铝与盐酸反应生成氯化铝和水,反应离子方程式为Al2O3+6H+=2Al3++3H2O;
铝与盐酸反应生成氯化铝与氢气,反应离子方程式为2Al+6H+=2Al3++3H2↑.
故答案为:Al2O3+6H+=2Al3++3H2O;2Al+6H+=2Al3++3H2↑;
(2)铝灰与过量的盐酸反应,过滤后收集滤液,加热浓缩至饱和,调pH值,稍静置,过滤收集滤渣,最终的这个滤渣就是我们要的晶体,所以生产过程中操作B和D的均为过滤.
故答案为:过滤、过滤;
(3)搅拌加热操作过程,加入盐酸,铝与盐酸反应,有氢气生成,加热的时候HCl会挥发,用水喷淋就可以吸收HCl,得到HCl(aq),剩余气体为氢气,反应中副产品a为H2.
故答案为:H2.
(4)95°C加热的时候HCl会挥发,用水喷淋就可以吸收HCl,得到HCl(aq),可进行循环使用.
故答案为:HCl;
(5)铝离子水解,Al3++3H2O?Al(OH)3+3H+,降低氢离子浓度促进铝离子水解,有利于聚合氯化铝晶体析出.
故答案为:促进AlCl3水解,使晶体析出;
(6)用氢氧化钠和氨水调节pH值,会引入新的杂质,引入钠离子和铵根离子.所以可以加入Al和氧化铝进行处理,它二者是固体,多了可以过滤掉的,所以可以使得到的晶体较纯净.
故答案为:BD.
本题解析:
本题难度:一般
2、实验题 (8分)某学生设计如下图Ⅰ装置,测定2 mol/L的硫酸与锌粒和锌粉反应的速率。请回答: 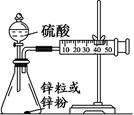 ?
?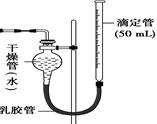 ?
?
图Ⅰ?图Ⅱ
(1)装置图Ⅰ中放有硫酸的仪器名称是?。
(2)按照图Ⅰ装置实验时,他限定了两次实验时间均为10 min,他还需要测定的另一个数据是 ?。
(3)实验结束后,得到的结论是?。
(4)该生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所在处的刻度数,发现滴定管中液面高于干燥管中液面,应首先采取的操作是?。
参考答案:(8分)?(1)分液漏斗?(2)收集到气体的体积
(3)其他条件相同时,锌粉比锌粒反应的速率快?(4)调节滴定管的高度使得两侧液面相平
本题解析:(1)根据装置的特点可知,装置图Ⅰ中放有硫酸的仪器名称是分液漏斗。
(2)要测定反应速率,则还需要测定的另一个数据收集到气体的体积。
(3)由于增大反应物的接触面积,可以加快反应速率,所以该实验中得出的结论是其他条件相同时,锌粉比锌粒反应的速率快。
(4)由于气体的体积受压强影响大,所以在读数之前还需要采取的措施是调节滴定管的高度使得两侧液面相平。
点评:该题是中等难度的试题,试题基础性强,注重对学生基础知识的巩固和训练,有利于调动学生的学习兴趣和学习积极性。该题试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
3、选择题 在图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是?
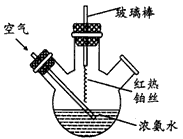
[? ]
A.反应后溶液中含有NO3-
B.反应后溶液中c(H+)增大
C.实验过程中有化合反应发生
D.实验过程中NH3・H2O的电离常数不可能发生变化
参考答案:D
本题解析:
本题难度:一般
4、简答题 某化学小组在实验中用浓硝酸和铜反应制取二氧化氮并探究二氧化氮是否能支持木炭的燃烧.其实验装置图如图所示:
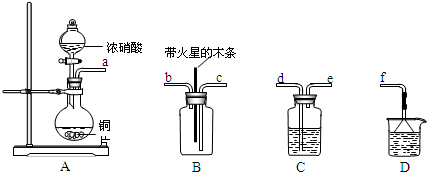
(1)按气流方向连接各仪器接口,顺序为a→______→______→______→______→f.
装置C、装置D的作用分别是______、______.
(2)实验开始后,能证明二氧化氮支持燃烧的实验现象是:______.
(3)等物质的量的二氧化氮和碳反应,生成两种气体物质,且其物质的量之比为1:1.该反应的化学方程式为:______.
参考答案:(1)本实验目的是制取二氧化氮并探究二氧化氮是否能支持木炭的燃烧,所以仪器连接顺序为:制取装置a、干燥装置C、二氧化氮与C反应装置B及吸收尾气装置D,仪器连接顺序为:a→d→e→c→b;二氧化氮是否支持燃烧的实验要求气体必须是干燥的,所以用装置C干燥二氧化氮气体;二氧化氮是有毒的气体,所以装置D用来吸收尾气,
故答案为:d;e;c;b;干燥气体;吸收尾气;
②根据装置B中带火星的木条燃烧,可以说明二氧化氮支持燃烧,故答案为:带火星的木条燃烧;
③生成的物质的量比为1:1有毒气体是一氧化氮和一氧化碳,反应的化学方程式为:NO2+C点燃.CO+NO,故答案为:NO2+C点燃.CO+NO.
本题解析:
本题难度:简单
5、实验题 (15分)乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。
乙酰苯胺的制备原理为: 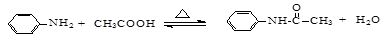
实验参数:
名称
| 式量
| 性状
| 密度/g/cm3
| 沸点/℃
| 溶解度
|
苯?胺
| 93
| 无色油状液体,
具有还原性
| 1.02
| 184.4
| 微溶于水
| 易溶于乙醇、乙醚等
|
乙?酸
| 60
| 无色液体
| 1.05
| 118.1
| 易溶于水
| 易溶于乙醇、乙醚
|
乙酰苯胺
| 135
| 白色晶体
| 1.22
| 304
| 微溶于冷水,溶于热水
| 易溶于乙醇、乙醚
|
实验装置:(见右图)
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
实验步骤:?
步聚1:在100ml圆底烧瓶中加入无水苯胺9.1mL,冰醋酸17.4mL,锌粉0.1g,安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,
调节加热温度,使柱顶温度控制在105℃左右,反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步聚2: 在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有100mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步聚3: 将此粗乙酰苯胺进行重结晶,待结晶完全后抽滤,尽量压干滤饼。产品放在干净的表面皿中晾干,称重,计算产率。
请回答下列问题:
(1)实验中加入锌粉的目的是???
(2)为何要控制分馏柱上端的温度在105?C左右???
(3)通过什么现象可判断反应基本完成???
(4)步聚1加热可用???(填“水浴”或“油浴”),步聚2中结晶时,若冷却后仍无晶体析出,可采用的方法是?。
(5)洗涤乙酰苯胺粗品最合适的试剂是 ???。
A. 用少量冷水洗? B. 用少量热水洗
C. 先用冷水洗,再用热水洗?D. 用酒精洗
(6)该实验最终得到纯品8.1克,则乙酰苯胺的产率是?。
参考答案:(1)防止苯胺在反应过程中被氧化;
(2)不断分出反应过程中生成的水,促进反应正向进行
(3)温度计温度下降或锥形瓶内液体不再增加;
(4)油浴;用玻璃棒摩擦容器内壁(或投入晶种或用冰水冷却);
(5)A?;(6)60%
本题解析:(1)苯胺不稳定,容易内空气中的氧气氧化为硝基苯,为防止苯胺在反应过程中被氧化;加入还原剂Zn粉。(2)水的沸点是100℃,加热至105℃左右,就可以不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率。(3)若看到温度计温度下降或锥形瓶内液体不再增加就表面反应物的蒸气较少,生成物达到了最大量,反应基本完成;(4)(4)由于步聚1加热的温度在105℃左右,而沸腾的水温度为100℃,不能达到该温度,所以步骤1可用油浴加热的方法。步聚2中结晶时,若冷却后仍无晶体析出,可采用的方法是用玻璃棒摩擦容器内壁(或投入晶种或用冰水冷却)的方法实现结晶;(5)由于乙酰苯胺微溶于冷水,溶于热水,所以洗涤粗品最合适的试剂是用少量冷水洗,以减少因洗涤造成的损耗。故选项为A。(6)n(苯胺)=" (9.1mL" ×1.02g/ml)÷93g/mol=0.1mol;n(乙酸)=( 17.4mL ×1.05g/ml)÷60g/mol=0.305mol。大于苯胺的物质的量,所以产生乙酰苯胺的物质的量要以不足量的苯胺为原料为标准。理论产量为0.1mol,而实际产量n(乙酰苯胺)= 8.1g÷135g/mol=0.06mol。所以乙酰苯胺的产率为0.06mol÷0.1mol×100%=60%。
本题难度:一般