1、选择题 下列变化不属于氧化还原反应的是
A.加热氢氧化铁固体
B.金属钠露置于空气中
C.铜丝放入浓硫酸中并加热
D.将氯气通入冷的消石灰浊液中
参考答案:A
本题解析:A.2Fe(OH)3 Fe2O3+3H2O,反应前后元素的化合价没有变化,不属于氧化还原反应。正确。B.4Na+O2=2Na2O.反应前后元素的化合价发生了变化,属于氧化还原反应。错误。C.Cu+2H2SO4(浓)
Fe2O3+3H2O,反应前后元素的化合价没有变化,不属于氧化还原反应。正确。B.4Na+O2=2Na2O.反应前后元素的化合价发生了变化,属于氧化还原反应。错误。C.Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。反应前后元素的化合价发生了变化,属于氧化还原反应。错误。D.2Cl2+ 2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O. 反应前后元素的化合价发生了变化,属于氧化还原反应。错误。
CuSO4+SO2↑+2H2O。反应前后元素的化合价发生了变化,属于氧化还原反应。错误。D.2Cl2+ 2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O. 反应前后元素的化合价发生了变化,属于氧化还原反应。错误。
本题难度:一般
2、选择题 氧化还原反应的实质是
A.氧元素的得失
B.氢元素的得失
C.电子的得失或偏移
D.元素化合价的升降
参考答案:C
本题解析:氧化还原反应的实质是电子的得失或偏移。其特征是某种元素或某些元素的化合价发生变化。
本题难度:简单
3、选择题 工业上制取氮化硅的化学反应原理是3Si+2N2 R(氮化硅)则R的化学式为
R(氮化硅)则R的化学式为
A.SiN
B.NSi
C.Si3N4
D.N4Si3
参考答案:C
本题解析:根据质量守恒定律计算,R的化学式为Si3N4。故选C。
点评:本题考查的是质量守恒定律、化学方程式的计算的相关知识,题目难度不大,平时多注意基础知识的学习。
本题难度:简单
4、计算题 (6分)用MnO2和浓盐酸反应制Cl2,当有0.4molHCl被氧化时,生成的Cl2全部用石灰水吸收,则
(1)制氯气的反应中转移了多少个电子?
(2)生成多少升氯气?
可制得漂白粉多少克?
参考答案:(1)2.048×1023 (2)4.48L (3)25.4g
本题解析:
试题解析:(1)MnO2+4HCl(浓) MnCl2+Cl2+2H2O↑,当有0.4molHCl被氧化时,反应转移了0.4mol电子,则转移电子数为2.048×1023个;(2)在MnO2+4HCl(浓)
MnCl2+Cl2+2H2O↑,当有0.4molHCl被氧化时,反应转移了0.4mol电子,则转移电子数为2.048×1023个;(2)在MnO2+4HCl(浓) MnCl2+Cl2+2H2O↑反应中,当有0.4molHCl被氧化时,生成氯气0.2mol;
MnCl2+Cl2+2H2O↑反应中,当有0.4molHCl被氧化时,生成氯气0.2mol;
(3)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2mol 111g 143g
0.2mol 11.1g 14.3g
则所得漂白粉的质量为11.1g+14.3g=25.4g。
考点:电子转移数目、化学方程式的计算
本题难度:一般
5、选择题 关于氧化还原反应CuO+H2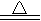 Cu+H2O,下列说法中正确的是
Cu+H2O,下列说法中正确的是
A.CuO是还原剂,H2是氧化剂
B.CuO是氧化剂,H2是还原剂
C.反应中Cu的化合价没有改变
D.反应中H的化合价没有改变
参考答案:B
本题解析:反中铜的化合价由+2价降至0价,得电子,被还原,氧化铜为氧化剂;氢元素化合价由0价升至+1价,失电子,被还原,氢气为还原剂。答案为B
本题难度:简单