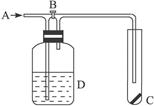
1、选择题 下图是一种试验某气体化学性质的实验装置,图中B为开关。如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是(? )
A.浓H2SO4
B.饱和NaCl溶液
C.浓NaOH溶液
D.浓NaBr溶液
参考答案:B
本题解析:本题主要考查氯气的漂白原理。当B开关打开时,干燥Cl2直接进入C试管,布条不褪色;当B开关关闭时,Cl2先进入D瓶,由于C、D选项中的物质都可以和Cl2反应,Cl2不会进入C试管;A选项进入C试管的依然是干燥的Cl2,布条不能褪色;饱和NaCl溶液不能和Cl2反应,而Cl2会带出溶液中的水,潮湿的Cl2使布条褪色。
本题难度:简单
2、选择题 为了在实验室制得不含氯化氢的干燥的氯气,正确的净化顺序是?(?)
A.第一步通过浓硫酸,第二步通过无水氯化钙
B.第一步通过碱石灰,第二步通过浓硫酸
C.第一步通过饱和食盐水, 第二步通过无水氯化钙
D.第一步通过水,第二步通过氧化钙
参考答案:C
本题解析:实验室制取的氯气中含有HCL、水蒸气,要得到干燥纯净的氯气,正确的净化顺序为第一步通过饱和食盐水,除去HCL气体,第二步通过无水氯化钙除去水蒸气;
本题难度:一般
3、实验题 某同学用下面的装置制备并收集纯净的氯化铁,硬质玻璃管E中装有细铁丝网。
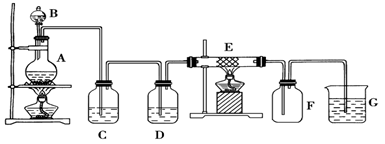
试回答:
(1)检验装置A的气密性的方法是?
(2)装置A中反应的化学方程式为?
(3)装置C的作用是:? ________________,装置D中的试剂是:____?_______。
(4)可检验装置E中生成的物质中阳离子的方法及现象是?。
(5)若把氯气通入石蕊溶液中,观察的现象是:?。
(6)装置 G中发生反应的离子方程式为:________________? _?____________。
参考答案:
(1)用酒精灯微热圆底烧瓶,一段时间后,C中导管冒气泡,停止加热后,导管中水柱回流一段,说明气密性好。(2分)
(2)4HCl(浓)+MnO2 = MnCl2+Cl2↑+2H2O(?加热条件)(3分)
(3)吸收HCl,浓硫酸?(各1分)
(4)硫氰化钾溶液(苯酚溶液、氢氧化钠溶液),显红色(紫色、产生红褐色沉淀)。(2分)
(5)先变红后褪色?(1分)
(6)Cl2+2OH-=Cl-+ClO-+H2O?(3分)
本题解析:该题是一道综合利用氯气的题,从制气到净化气到检验氯气的性质到最后的尾气处理。
本题难度:一般
4、选择题 下列有关元素及其化合物知识的说法中正确的是(? )
A.浓硝酸能与木炭反应,证明浓硝酸既具有强氧化性又具有强酸性
B.溴中溶有少量氯气,可用先加入少量溴化钠溶液再用酒精萃取的方法提纯
C.高温下SiO2与Na2CO3反应生成Na2SiO3和CO2,证明硅酸酸性强于碳酸
D.铵盐受热都能分解,但不一定都能生成氨气
参考答案:D
本题解析:A项中只证明了硝酸的强氧化性,A错误;B项中酒精易溶于水,不能用酒精萃取溴,B错误;C项中的反应能进行是因为生成了CO2气体,并不能证明硅酸酸性强于碳酸,C错误;D项中硝酸铵等铵盐受热分解一般不产生氨气,D正确
本题难度:一般
5、选择题 用含4 mol HCl的浓盐酸与足量的MnO2共热,生成的氯气为(?)
A.2 mol
B.1 mol
C.小于1 mol
D.小于2 mol,大于1 mol
参考答案:C
本题解析:4HCl(浓)+MnO2====MnCl2+Cl2↑+H2O
4 mol? 1 mol
随着反应的进行,浓盐酸的浓度变稀,反应停止,所以生成Cl2小于1 mol。
本题难度:简单