1���ƶ��� ��������AΪdz����ɫ�ᾧ����һ����Ҫ�Ļ�ѧ�Լ����������ۺϴ�����A����Һ��������ת����ϵ

�ش��������⣺
��1����ɫ����C�Ļ�ѧʽΪ_____________����ɫ����E�ĵ���ʽΪ_________________��
��2����Dת����ΪF�Ļ�ѧ��Ӧ����ʽΪ_________________��
��3����ȡһ����A�ľ��壬���ⶨ��ᾧˮ����ԼΪ27.6%��������ȫ����ˮ�����Һ����������ת�����ɵõ���C��F�����ʵ���֮��Ϊ2�U1���ɴ˿�ȷ��A�Ļ�ѧʽΪ_______________��
��4������ת����ϵ�У�����ϡ�������ϡ���ᣬ_________����ܡ����ܡ���ͨ����ת����ϵȷ��A����ɣ�������_______________________��Ҫȷ�Ƴ�C����������Ҫ�ظ����и����ȴ�������IJ�����Ŀ����_____________________��
��5��A�ı���Һ�������ڱ궨���������Һ�ȡ���д���ڸ��������Һ�еμ�A�ı���Һʱ�������������ӷ�Ӧ����ʽ������������ת�������________________________��
�ο��𰸣���1��BaSO4��
��2��4Fe(OH)2+O2+2H2O = 4Fe(OH)3
��3��(NH4)2Fe(SO4)2��6H2O
��4�����ܣ���Ϊ����ȷ�����������λ����������Σ����׳�ȥC�����ˮ��
��5��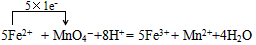
���������
�����Ѷȣ�һ��
2������� ��15�֣��ѣ�Ti������Ϊ��������֮��ĵ�������������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ���С������Ⱦ������д���пհף�

��1����ⱥ��ʳ��ˮʱ���÷�Ӧ�����ӷ���ʽ��____________________��
��2����֪����Mg(s)��Cl2(g)=MgCl2(s);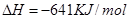
��

�� ____________
____________
��Ӧ��

 ��Ar������������________
��Ar������������________
��3��д���������뽹̿��Cl2�����Ƶ����Ȼ��ѵĻ�ѧ����ʽ______________________
��4���Լ״�������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء���֪��ȼ�ϵ�ص��ܷ�ӦʽΪ��2CH3OH��3O2��4OH��=2CO32����6H2O����ȼ�ϵ�ط�����Ӧʱ��������Һ��PH_____�����������С�����䡱���õ���и����ϵĵ缫��Ӧ��__________.
��5����������ҵ���кϳ�96t�״�����������H2_________t���������������������ʵ��κ���ʧ��
�ο��𰸣���1����2�֣�2Cl����2H2O  Cl2����H2����2OH��?
Cl2����H2����2OH��?
��2����512 KJ/mol ��2�֣�
Mg��Ti���н�ǿ��ԭ�ԣ��ڸ����¶���������е�O2��Ӧ��2�֣�
��3��2FeTiO3��6C��7Cl2 2FeCl3��2TiCl4��6CO��3�֣�
2FeCl3��2TiCl4��6CO��3�֣�
��4������2�֣�? CH3OH��6e����8OH��=CO32����6H2O��2�֣�?��5��12?��2�֣�
�������������1�����ʳ��ˮ����NaOH��H2��Cl2��
���ø�˹����2��-�ڼ��ɼ������Ӧ��Ϊ��512 KJ/mol������Mg��Ti���н�ǿ��ԭ�ԣ��ڸ����¶���������е�O2��Ӧ�����Է�ӦҪ��Ar�����н��С�
��3�ڼ��Ի����������� O2 + 4e- + 2H2O= 4OH- ���������������ļ�����ǿ�������״�����������Ӧ��CH3OH��6e����8OH��=CO32����6H2O
��5��CO(g)��2H2(g)���� CH3OH(g)
4?32
X? 96t
x="12" t
������������ѧ������Ϥ�Ľ����ѣ�Ti��Ϊ���ۣ���ϻ�ѧ���գ������֪ʶ��㣬������Ƶ�֪ʶ���ע�ضԻ���֪ʶ��Ŀ��顣
�����Ѷȣ�һ��
3������� ��ͼΪ��ѧ�������ʼ��ת����ϵ�����мס��ҡ�������Ϊ���ʣ�����Ϊ�������������Ԫ������������������������C������Ϊ��ɫҺ�壬B��ɫ��ӦΪ��ɫ��һЩ����Һ�н��еķ�Ӧ��Һ�е�H2O�����ɵ�H2O��ʡ�ԡ�
�ش��������⣺
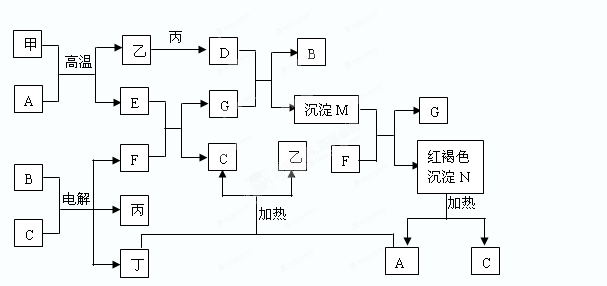
��1������������Ԫ�������ڱ��е�λ��______________________��
��2��������F�ĵ���ʽ________________________��
��3��D��G��Ӧ�����ӷ���ʽ___________________________________��
��4����A��Ӧ�Ļ�ѧ����ʽ___________________________________�����෴Ӧһ�㱻����________��Ӧ���÷�Ӧ����ҪӦ��_________________��(2��)
�ο��𰸣���1���������ڣ�����? (2��)? (дһ�벻����)
��2��
��3��Fe3����3AlO2����6H2O��Fe(OH)3����3Al(OH)3��? (2��)? (��ѧʽ1�֣���ƽ1��)
��4��2Al��Fe2O3  ?Al2O3��2Fe? (2��)? (��������1��)?���ȡ�(2��)�����Ӹֹ졡ұ�����۽���? (2�֣�ÿ��1��)
?Al2O3��2Fe? (2��)? (��������1��)?���ȡ�(2��)�����Ӹֹ졡ұ�����۽���? (2�֣�ÿ��1��)
����������ס��ҡ�������Ϊ���ʣ�����Ϊ�������������Ԫ��������������������������Ϊ����C������Ϊ��ɫҺ�壬CΪˮ��NΪ���ɫ���壬NΪFe��OH��3��Fe��OH��3���ȷֽ�������������ˮ����AΪ�����������ת����ϵͼ��������ʵ����ʣ�����֪����Ϊ������Ϊ������Ϊ��������Ϊ������AΪ��������BΪ�Ȼ��ƣ� CΪˮ��DΪ�Ȼ�����EΪ��������FΪ�������ƣ�GΪƫ�����ƣ�MΪ�������������������Ļ�����1��������Ϊ��������Ԫ�������ڱ��е�λ�õ������ڣ����壻��2��������FΪ�������ƣ�����ʽΪ?����3���Ȼ�����Һ��ƫ��������Һ��Ӧ�����ӷ���ʽΪFe3����3AlO2����6H2O��Fe(OH)3����3Al(OH)3������4��������������Ӧ�Ļ�ѧ����ʽΪ2Al��Fe2O3 �� Al2O3��2Fe �����෴Ӧһ�㱻�������ȷ�Ӧ���÷�Ӧ����ҪӦ�ú��Ӹֹ졡ұ�����۽�����
�����Ѷȣ�����
4������� ��8�֣���ͼ��A��J��Ϊ��ѧ��ѧ�г��������ʣ�����֮��������ת����ϵ������A��DΪ�����������ʣ�B��CΪ���������HΪ��ɫ������IΪ���ɫ������(��Ӧ���������ɵ�ˮ��������������ȥ)
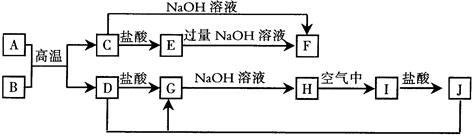
��ش��������⣺
��1��A��Ԫ�����ڱ��е�λ����?���ڴ��ģ��ҵ�����У���Bұ��
D��ʹ�õĻ�ԭ����?��
��2��д����Ӧ��J+D��G�������ӷ���ʽ��?��ʵ����Ҳ���Խ�Gֱ��ת��ΪJ�����õ��Լ�Ϊ?��
��3��C��NaOH��Һ��Ӧ��E�������NaOH��Һ��Ӧ�������֮һ����AԪ�أ���
������AԪ�صĴ�����ʽΪ?���û�ѧ���ű�ʾ����
�ο��𰸣���1���������� IIIA��?��2�֣�? CO?��1�֣�
��2��Fe+2Fe3+=3Fe2+?��2�֣���ˮ?��1�֣�?��3��AlO2-?��1�֣�
���������������������ͼ�⣬��������ͻ�Ƶ㡣IΪ���ɫ��������IΪ������������HΪ������������GΪ�Ȼ�������DΪ��������A��B��Ӧ��������֪����ӦΪ���ȷ�Ӧ������AΪ����CΪ��������EΪ�Ȼ�����FΪƫ�����ơ�
�����Ѷȣ�һ��
5��ѡ���� A��B��C�ֱ���Ԫ�ؼס��ҡ����ĵ��ʣ����Ƕ��dz����Ľ�����ǽ�����D��E��F�dz��������������������ͼ��ʾת����ϵ��������˵������ȷ���ǣ�������
A��D��E��һ�������м�Ԫ��
B������B�϶���������
C��A��B��C��һ����һ������Ԫ�صĵ���
D����A�Ƿǽ�������Bһ��Ϊ����
