1、选择题 氟、氯、溴、碘四种元素,它们的下列性质的递变规律不正确的是(? )
A.单质密度依次增大
B.单质的熔沸点依次升高
C.Cl2可以从KBr溶液置换出Br2
D.F2可以从NaCl溶液中还原出Cl2
参考答案:D
本题解析:根据卤素单质的物理性质递变规律可知,选项AB正确;同主族自上而下非金属性逐渐减弱,所以根据较强的非金属单质能置换出减弱的非金属单质可知,选项C正确。由于F是最强的非金属元素,极易和水反应,所以F2不能从NaCl溶液中还原出Cl2,D不正确,答案选D。
点评:该题是基础性试题的考查,也是高考中的常见题型。试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力,提升学生的学科素养。
本题难度:一般
2、选择题 世界卫生组织(WHO)将ClO2?列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛的应用.ClO2属于
A.酸
B.碱
C.氯化物
D.氧化物
参考答案:D
本题解析:分析:A、电离时生成的阳离子都是氢离子的化合物是酸;
B、电离时生成的阴离子都是氢氧根离子的化合物是碱;
C、氯化物是负价氯和另外一个化学元素组成的二元化合物.
D、氧化物是负价氧和另外一个化学元素组成的二元化合物.
解答:二氧化氯是由氯元素和氧元素组成的化合物,氯元素为+4价,氧元素为-2价,属于氧化物.
故选:D.
点评:考查物质的分类方法,难度不大,注意氧化物氧化物是负价氧和另外一个化学元素组成的二元化合物.
本题难度:困难
3、选择题 在自然界中以游离态存在的金属是
A.铁
B.金
C.钠
D.铝
参考答案:B
本题解析:活泼性强的金属以化合态存在自然界中,活泼性弱的金属以游离态形式存在自然界中,故选B。
点评:本题考查的是金属在自然界中的存在形态,学生学过的金属活动顺序表中靠前的以化合态形态存在,靠后的以游离态形态存在。
本题难度:一般
4、填空题 已知A~N分别代表一种物质,它们之间的转化关系如图所示(部分反应的反应条件和生成物已略去)。A、B、C分别是由短周期元素组成的单质,A是金属,D是无色液体。F是一种离子化含物,其阴阳离子的个数比为1:3,且能与水反应得到两种碱。反应①是实验室检验某离予的方法,反应②是工业、生产N的重要反应。请回答下列问题:
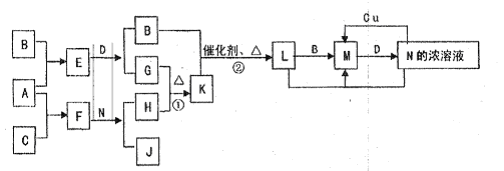
(1)B元素在元素周期表中的位置是?,F的电子式是?。
(2)写出反应①的离子方程式:
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是?
(请用上图所示关系中反应的化学方程式回答)。
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法。亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO・bCr2O3等,统称为亚铬酸铜。
CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的
化学方程式:?。
(5)已知一定温度(>100℃)下,反应②的平衡常数为1。将0.8 mol K和1.1mol B放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4 mol/L,此时反应v正?v逆(填“>”、“<”或“=”)。 当反应到达平衡后,保持温度不变,再加入一定物质的量的B,重新达到平衡,则L的平衡浓度?(填“增大”、“不变”或“减小”),B的转化率
? _。(填“升高”、“不变”或“降低”),L的体积分数?(填“增大”、“不变”、“减小”或“无法确定”)。
参考答案: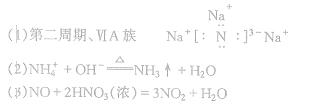

本题解析:略
本题难度:一般
5、选择题 X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是
?
A.Y元素最高价氧化物对应的水化物化学式为H2YO3
B.原子半径由小到大的顺序为:Y<X<W<Z
C.室温下,Z和W的单质均能溶于浓硝酸
D.X、Z两种元素的氧化物中所含化学键类型相同
参考答案:B
本题解析:X、Y、Z、W为C、N、Mg、Al。A、N对应的最高价氧化物对应的水化物化学式为HNO3,错误;B、电子层数多半径大,同周期从左到右原子半径减小,正确;C、常温下铝在浓硫酸、浓硝酸中钝化,错误;D、对应的氧化物为二氧化碳和氧化镁,分别为共价化合物和离子化合物,错误。
本题难度:一般