|
高考化学知识点归纳《原电池原理》试题预测(2020年最新版)(六)
2025-06-25 22:50:16
【 大 中 小】
|
1、填空题 (11分)
(1)海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
①写出氯化镁的电子式__________________________
②重水的摩尔质量为____________________________
③写出金属镁的工业冶炼方程式__________________________________________
④海水淡化的常见方法有电渗析法、离子交换法、_________________
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是____________________________
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是________(填选项)
A.沸点低
B.沸点高
C.易挥发
D.难挥发
| ③甲烷与氯气光照下反应生成产物共________种
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是
参考答案:
(1)①? ?(1分) ?(1分)
②? 20 g/mol?(单位不写不给分)?(1分)
③? MgCl2(融熔) Mg+Cl2↑?(2分) Mg+Cl2↑?(2分)
④?蒸馏法?(1分)
(2) ① CH2=CH2+HCl CH3CH2Cl?(2分) CH3CH2Cl?(2分)
②? A? C?(2分)?
③ 5?(1分)
(3) CH4?(写名称也可)?(1分)
本题解析:
(1)② 分子式D2O
③ 电解熔融氯化镁,电能转化为化学能。 熔融氯化镁, 电解熔融状态下的氯化镁生成物是氯气和金属镁。
② 沸点低,蒸发时需吸收大量的热,可使受伤部位的温度迅速降低,从而达到局部冷冻麻醉的目的。
③甲烷与氯气反应生成一氯甲烷,二氯甲烷,三氯甲烷,四氯甲烷(即四氯化碳)和氯化氢,只有一氯甲烷和氯化氢是气态产物
本题难度:一般
2、选择题 关于下图装置的叙述,正确的是
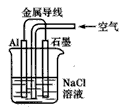
[? ]
A.铝是负极,铝片上析出无色气体
B.石墨是负极,石墨棒上析出黄绿色气体
C.溶液中两电极间产生白色沉淀
D.溶液中先产生白色沉淀,最后沉淀溶解
参考答案:C
本题解析:
本题难度:一般
3、选择题 人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为 Zn+2OH--2e-=ZnO+H2↑,
Ag2O+H2O+2e-==2Ag+2OH-。据此判断Ag2O是
[? ]
A.负极,被氧化
B.正极,被还原
C.负极,被还原
D.正极,被氧化
参考答案:B
本题解析:
本题难度:一般
4、选择题 关于原电池的说法,正确的是( )
A.在正极上发生氧化反应
B.某电极上有氢气产生,则此电极为正极
C.在外电路上电子流出的为正极
D.在负极上发生还原反应
参考答案:A.原电池的正极上得到电子,发生还原反应,故A错误;
B.有氢气生成,则氢离子得电子,所以该电极为正极,故B正确;
C.电子由负极流向正极,所以在外电路上电子流出的为负极,故C错误;
D.原电池的负极上失去电子,发生氧化反应,故D错误;
故选B.
本题解析:
本题难度:一般
5、填空题 (8分)根据原电池的知识回答下列问题
(1)图一烧杯中溶液为稀硫酸,则观察到Al上的现象是
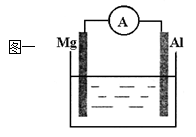
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应为: 。
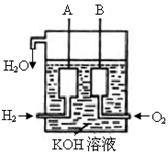
(3)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电 池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为: 。
(4)铅蓄电池放电时反应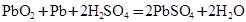 ,若放电消耗2mol硫酸时电路中转移电子_________mol ,若放电消耗2mol硫酸时电路中转移电子_________mol
参考答案:(1)产生大量气泡 (2)O2+2H2O+4e-=4OH-
(3)CH4+10OH-―8e-=CO32-+7H2O (4)2mol (1分)
本题解析:(1)在原电池中较活泼的金属作负极,不活泼的金属(非金属)作正极。因为镁的活泼性强于Al的,所以若用稀硫酸作电解质溶液,则镁是负极,铝是正极,溶液中的氢离子在正极上得到电子,被还原生成氢气。
(2)在燃料电池中,氧气得到电子,所以氢气等燃料在负极通入,氧气(或空气)在正极通入,因此正极反应式为O2+2H2O+4e-=4OH-。
(3)甲烷在反应中失去电子,被氧化生成CO2和水,但电解质是氢氧化钾溶液,所以生成的CO2被吸收,生成碳酸钾。所以负极的电极反应式为CH4+10OH-―8e-=CO32-+7H2O。
(4)根据总反应式可判断,铅是还原剂,化合价有0价升高到+2价,失去2个电子,所以每消耗2mol硫酸,反应中转移的电子是2mol。
本题难度:一般
|