1��ѡ���� ���д�ʩ��Ϊ�˽��ͻ�ѧ��Ӧ���ʵ��ǣ�������
A����ʯ��ʯ������ϸ�������ᷴӦ
B����MnO2��H2O2�ֽⷴӦ�Ĵ���
C��ʳƷ���ڱ���������
D�������ռ���Һ��Ӧʱ��������
�ο��𰸣�A����ʯ��ʯ������ϸ������Ӵ�������ܼӿ췴Ӧ���ʣ���A����
B���������̷�ĩ���������ܼӿ����������Һ�������ķ�Ӧ���ʣ���B����
C����ʳ�������ڱ����У��¶Ƚ��ͣ��ܼ�����Ӧ���ʣ���C��ȷ��
D�������ռ����Ӧʱ�����ȣ������¶Ȼ�ӿ����������ķ�Ӧ���ʣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
2��ѡ���� ���ڿ��淴Ӧ��2A(��)��B(��) 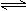 ?2C(��)�� ��H��0�����и�ͼ��ȷ����
?2C(��)�� ��H��0�����и�ͼ��ȷ����
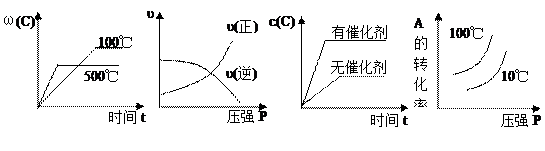
A? B? C? D
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3������� ��þ��Ͷ��ʢ���ڳ������������������H2��������?ʱ��Ĺ�ϵ����ͼ��ʾ��
��1��д�����ӷ�Ӧ����ʽ______
��2�������������Т�H+��Ũ��?��þ���ı����?����Һ���¶�?��Cl-��Ũ�Ȳ���Ӱ��÷�Ӧ���ʵ�������______������ţ���
��3������ͼ��AB���γɵ�ԭ��______��
��4������ͼ��t1ʱ�̺����ʱ�С��ԭ��______��
�ο��𰸣���1��þΪ���ý��������ᷴӦ������������Ӧ�����ӷ���ʽΪMg��s��+2H+�TMg2++H2�����ʴ�Ϊ��Mg��s��+2H+�TMg2++H2����
��2����Ӧ��ʵ����Mg��s��+2H+�TMg2++H2������H��0����Ӧ���ʳ���������Ũ�����⣬�����ĸ����ضԷ�Ӧ���ʶ���Ӱ�죬�ʴ�Ϊ���ܣ�
��3����Ӧ���ȣ������¶������ߣ��¶����ߣ���Ӧ�������ʴ�Ϊ����Ӧ���ȣ��¶����ߣ���Ӧ��������
��4�����ŷ�Ӧ�Ľ��У���Ӧ���Ũ����С����Ӧ���ʼ�С���ʴ�Ϊ����Ӧ���Ũ����С��
���������
�����Ѷȣ�һ��
4������� ̽����������Ի�ѧ��Ӧ���ʵ�Ӱ�쳣�õ��÷�Ӧ
��֪��Na2S2O3+H2SO4��Na2SO4+S��+SO2+H2O
���������Ӧ�漰����Ԫ�ػ����ʼ����ʻش��й����⣺
23����Ԫ�صĻ��ϼ��ɸߵ���˳��Ϊ��______________________________
�漰Ԫ�صļ����Ӱ뾶��С����˳��Ϊ��______________________________;
24����ԭ�ӵ����������Ų������ʾʽ��______________________________;
�о�2����˵������������Ԫ�طǽ�����ǿ����ʵ��______________________________;
25.Ԥ��þ�ڶ���������ȼ�յ�����________________________________________
���������þ������������ ���ɡ�
26.������ijͬѧ�Ǹ��ݸ÷�Ӧʵ�����ݻ��Ƶ�ͼ��
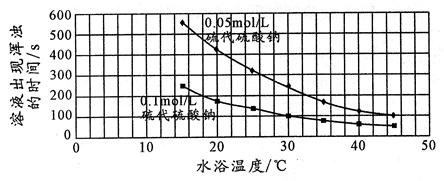
��ͬѧ�ó��Ľ����ǣ�
_________________________________________________________________________________��
27.��SO2ͨ��BaCl2��Һ�����ͣ�δ���������ɣ������μ�һ�����İ�ˮ������BaSO3�������õ���ƽ��ԭ��������������
_________________________________________________________________________________��
������ͨ��������������Cl2 ��H2SҲ��������������û�ѧ����ʽ��ʾ���ɳ�����ԭ����
_________________________________________________________________________________��
�ο��𰸣�23.+6��+4��+2��0 �� H+
���������
�����Ѷȣ�����
5��ѡ���� Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬���д�ʩһ������߷�Ӧ���ʵ��ǣ�?��
A���ı䷴Ӧ������
B����Сѹǿ
C�������¶�
D�������¶�
�ο��𰸣�D
�����������
�����Ѷȣ���