微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下存在下列平衡:2A(g)?B(g);△H<O在测定A的相对分子质量时,下列条件中测定结果误差最小的是( )
A.温度150℃、压强5.05×104Pa
B.温度150℃、压强4.04×105Pa
C.温度25℃、压强1.01×105Pa
D.温度0℃、压强5.05×104Pa
参考答案:由于存在平衡2A(g)?B(g),B的存在会影响A的相对分子
本题解析:
本题难度:一般
2、简答题 (14分)研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:①Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g) △H 1 = +489.0 kJ・mol-1
②C(石墨) +CO2(g) = 2CO(g) △H 2 = +172.5 kJ・mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的ΔH 0 (填“>”、“<”或“=”)。
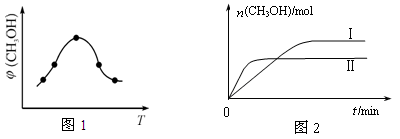
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 。
当氨碳比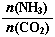 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为 。
参考答案:(1)Fe2O3(s)+3CO(g) = 2Fe(s)+3C
本题解析:
试题分析:(1) ①-②×3,整理可得Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H = ―28.5 kJ/mol。(2)①化学平衡常数是可逆反应达到平衡状态时各种生成物浓度的幂指数的乘积与各种反应物浓度的幂指数的乘积的比。对该反应来说,K=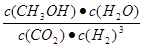 。②由甲醇的体积分数φ(CH3OH)与反应温度T的关系图示可知:当反应达到平衡后,升高温度,甲醇的体积分数减小,说明升高温度,化学平衡逆向移动。根据偏高移动原理:升高温度梦幻西游平衡向吸热反应方向移动。逆反应方向为吸热反应,所以正反应为放热反应。所以ΔH<0。 ③曲线Ⅱ比I先达到平衡。说明温度温度曲线Ⅱ>I。由于温度高,CH3OH含量低,说明化学平衡常数KⅠ>KⅡ。(3)①根据质量守恒定律,由CO2和NH3在一定条件下合成尿素[CO(NH2)2]的反应方程式为2NH3+CO2
。②由甲醇的体积分数φ(CH3OH)与反应温度T的关系图示可知:当反应达到平衡后,升高温度,甲醇的体积分数减小,说明升高温度,化学平衡逆向移动。根据偏高移动原理:升高温度梦幻西游平衡向吸热反应方向移动。逆反应方向为吸热反应,所以正反应为放热反应。所以ΔH<0。 ③曲线Ⅱ比I先达到平衡。说明温度温度曲线Ⅱ>I。由于温度高,CH3OH含量低,说明化学平衡常数KⅠ>KⅡ。(3)①根据质量守恒定律,由CO2和NH3在一定条件下合成尿素[CO(NH2)2]的反应方程式为2NH3+CO2 CO(NH2)2+H2O。
CO(NH2)2+H2O。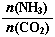 =3,假设n(CO2)=amol,则n(NH3)=3amol。由于达平衡时CO2的转化率为60%,所以反应消耗的n(CO2)=0.6amol.,根据方程式中二者的物质的量的关系可知反应的NH3的物质的量n(NH3)=1.2amol.所以氨气的转化率为(1.2amol.÷3amol)×100%=40%.②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,则根据题意可得:该电极反应的方程式为CO2+8e―+8H+=CH4+2H2O。
=3,假设n(CO2)=amol,则n(NH3)=3amol。由于达平衡时CO2的转化率为60%,所以反应消耗的n(CO2)=0.6amol.,根据方程式中二者的物质的量的关系可知反应的NH3的物质的量n(NH3)=1.2amol.所以氨气的转化率为(1.2amol.÷3amol)×100%=40%.②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,则根据题意可得:该电极反应的方程式为CO2+8e―+8H+=CH4+2H2O。
考点:考查热化学方程式的书写、化学平衡常数的表达式、温度对化学平衡常数的影响、物质转化率、电化学电极式的书写的知识。
本题难度:困难
3、填空题 氮和硫是参与自然界循环的重要元素,并建立了平衡。如果这种循环平衡遭到破坏,将导致环境灾难,从而危害人类的生存。
(1)在一定温度下,体积恒定的密闭容器中,二氧化氨和二氧化硫会发生如下反应:
NO2(g)+SO2(g)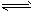 NO(g)+SO3(g)
NO(g)+SO3(g)
①该反应的平衡常数表达式为____________。
②在上述平衡体系中通入少量O2,NO的浓度________,这是因为通入少量O2后,平衡向正反应方向移动,达到新的平衡时与原平衡比较,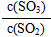 _______,
_______, ________,而c(NO)与c(NO2)之和
________,而c(NO)与c(NO2)之和
____(填“增大”“减小”或“不变”)。
(2)如果将一定量二氧化氮和二氧化硫混合于某2L密闭容器中,在一定温度下反应,10 min时立即将容器内气体的温度冷却到标准状况,得到0.6 g同体。则10 min内NO2的平均反应速率为____________。
(3)请用上述反应中的某种生成物的有关物理量来说明该反应已达到平衡状态:
①_____________________;②____________________。
参考答案:(1)①![]() 本题解析:
本题解析:
本题难度:一般
4、选择题 一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g)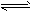 zC(g)(正反应为放热反应);达到平衡后测得A气体的浓度为0.5 mol・L-1;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A的浓度为0.3 mol・L-1。则下列叙述正确的是[???? ]
zC(g)(正反应为放热反应);达到平衡后测得A气体的浓度为0.5 mol・L-1;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A的浓度为0.3 mol・L-1。则下列叙述正确的是[???? ]
A.平衡向右移动
B.x+y>z
C.B的转化率提高
D.C的体积分数增加
参考答案:B
本题解析:
本题难度:一般
5、选择题 在容积相同的两密闭容器A和B中,保持温度为150℃,同时向A容器中加入a mol HI,向B容器中加入b mol HI (a>b),当反应2 HI (g)  H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
A.从反应开始达到平衡,所需时间tA>tB
B.平衡时 C(I2)A= C(I2) B
C.平衡时I2 蒸气在混合气体中的体积分数:A>B
D.HI的平衡分解率aA=aB
参考答案:D
本题解析:
试题分析:A、容器中A中反应物的浓度大,反应速率大,达平衡需要的时间少,A错误;B、两容器中平衡时HI的转化率相同,A容器加入的物质少,平衡时 C(I2)A< C(I2) B,B错误;C、平衡时A、B中HI的转化率相同,设转化率为x,平衡时A容器中:HI物质的量为a-ax,H2和I2均为1/2ax;平衡时B容器中:HI物质的量为b-bx,H2和I2为1/2bx,体积百分含量(也就是物质的量的百分含量)为1/2x,所以是相同的,C错误;D、两容器中平衡时HI的转化率相同,D正确;选D。
考点:考查等效平衡。
本题难度:一般