微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 为测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,称取一定质量的样品,甲同学利用图I所示装置测量产生CO2的体积,乙同学利用图II所示装置通过干燥管的增重测量产生CO2的质量,已知所用稀硫酸均足量。
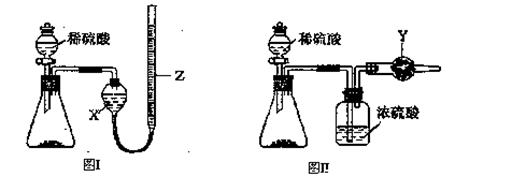
(l)盛放稀硫酸的仪器名称为 ???????????????????????。
(2)试剂X为??????????????????;试剂Y为??????????????????。
(3)甲同学在进行实验时,为减小误差,应注意的事项有(填选项字母)??????????。
A.读数前应使整套装置冷却至室温
B.调整Z的高度使量气装置左右液面相平
C.读数时视线与Z内凹液面最低点相切
D.读数前应通入一定量的N2使生成的CO2全部进入量气装置
(4)按乙同学的实验方案进行实验,使测得的Na2CO3的质量分数偏高的因素有(写一种)
???????????????????????????????????,使测得的Na2CO3的质量分数偏低的因素有
(写一种)???????????????????????????????。
(5)为完成相同的测定任务,下列实验方案不能达到实验目的的是??????????(填选项字母)。
A.取mg混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干得ng固体
B.取mg混合物与足量盐酸充分反应,将溶液加热、蒸干、灼烧得ng固体
C.取mg混合物充分加热,固体质量减少ng
D.将图II装置中的稀硫酸改为稀盐酸进行实验
参考答案:
(1)分液漏斗;
(2)饱和NaHCO3溶液;
本题解析:
试题分析:(2)饱和NaHCO3溶液中二氧化碳的溶解度较小。干燥管中只能装固态的干燥剂。(3)用排液法来测定气体的体积,要注意三点:一是温度要恢复到原来的温度,二是压强要恢复到原来的压强,三是读数时要平视。
(4)设混合物质总质量为ag,混合物中含Na2CO3的质量为xg,那么含NaHCO3的质量为(a-x)g,再设干燥管中吸收的二氧化碳的质量为bg.
Na2CO3 本题难度:一般
本题难度:一般
2、实验题 有人设计一个Na2O2与CO2反应实验装置图如下:
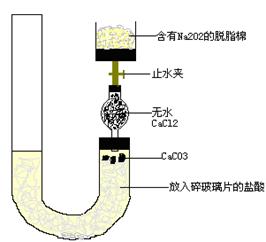
打开止水夹,发现CO2通过裹有Na2O2的脱脂棉,可观察到脱脂棉剧烈燃烧起来.
(1)由实验现象所得出的有关Na2O2与CO2反应的结论是:
a:有氧气生成:b:?????????????????????????????????
(2)甲、乙两位同学各称取质量为m g的过氧化钠与二氧化碳反应后的样品,并用下图所示仪器测定样品的组分。

请回答下列问题:
①甲同学通过实验测得的数据是氧气的体积,该同学读取实验数据时应注意冷却至室温、____________、眼睛视线与凹液面最低处相切。
②乙同学通过连接仪器①②进行实验,他测得的数据是?????????????。按他测得的数据计算出的实验结果偏高,理由是?????????????????????。
③为了测得准确的实验数据,请你将乙同学的实验装置进行改进(每种仪器只准使用一次),写出各仪器接口的连接顺序???????????????????????????。
④按③设计的实验装置进行实验,若测得实验前后装置②的质量分别是w1 g和w2 g,则样品中碳酸钠的质量分数为???????????????????????。
⑤在③的改进装置中由于受到仪器的局限,是否也有不足之处??????(若没有,此空不必回答;若有,请一并说出不足的理由)?????????????????。
参考答案:(1)b:该反应是放热反应。(2)①调节④⑥液面高度相同②二
本题解析:本题主要是探究Na2O2和CO2反应的实质。⑴Na2O2遇CO2能使脱脂棉剧烈燃烧起来,从燃烧的条件可知,必须有氧气生成,而且该反应还要放出大量的热。(2)本题涉及定量测气体体积与气体质量的区别。若通过实验测得氧气的体积,则应采用排液量气装置,因为反应生成的是氧气和二氧化碳的混合气体,先除杂,再量气。若通过实验测得二氧化碳的质量,则必须保证反应产生的二氧化碳全部被碱石灰吸收,但如果只连接①②,则反应产生的水蒸气以及空气中的水蒸气、二氧化碳也可能被碱石灰吸收,使结果偏大,如果改进应该在②前后分别加上干燥装置
本题难度:简单
3、选择题 下列叙述正确的是( )
A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
B.Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
C.NaCl与Na2CO3灼烧时火焰颜色不相同
D.Na2O2可作供氧剂,而Na2O不行
参考答案:D
本题解析:能和酸反应生成盐和水的氧化物是碱性氧化物,过氧化钠不是碱性氧化物,A不正确;碳酸氢钠和氯化钙是不反应的,选项B不正确;氯化钠和碳酸钠都含有钠元素,焰色反应是相同的,选项C不正确,所以正确的答案选D。
本题难度:一般
4、选择题 纯碱和小苏打都是白色晶体,在日常生活中都可以找到。若要在家中将它们区分开来,下面的方法中可行的是
A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度
B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色
C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀
D.分别放在炒锅中加热,观察是否有残留物
参考答案:A
本题解析:
试题分析:A.碳酸钠与酸反应分步进行,首先反应产生碳酸氢钠和氯化钠,然后是碳酸氢钠与酸反应产生碳酸钠二氧化碳和水,产生气体,而碳酸氢钠中加入酸马上放出气体,所以根据反应放出气体的快慢就可迅速得到判断。正确。B. 纯碱和小苏打都是钠盐,焰色反应火焰都为黄色。所以无法区别二者。错误。C.二者都能与氢氧化钙溶液发生反应产生碳酸钙白色沉淀,无法区别它们。错误。D.碳酸钠稳定,受热不分解,碳酸氢钠不稳定受热分解产生碳酸钠、二氧化碳和水,也有固体残留物,所以无法区分二者。错误。
本题难度:一般
5、选择题 中学化学实验中常用到碳酸钠溶液,下列有关叙述错误的是
A.在实验室中,能用碳酸钠溶液制备少量烧碱
B.实验室制CO2气体时,用饱和碳酸钠溶液除去其中混有的HCl气体
C.制取乙酸丁酯时,用于除去混有的丁醇和乙酸
D.做银镜反应实验时,可用热的碳酸钠溶液洗涤掉反应前试管内壁上的油污
参考答案:B
本题解析:
试题分析:A. Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH.因此在实验室中,能用碳酸钠溶液制备少量烧碱。正确。B.实验室制CO2气体时,CO2气体中常含有少量的HCl气体,可以用饱和碳酸氢钠溶液来除去。反应的方程式为NaHCO3+HCl=NaCl+H2O+ CO2↑。若要饱和的碳酸钠溶液,则还会发生反应:Na2CO3++H2O+ CO2= 2NaHCO3.使CO2气体也损耗。故错误。C.碳酸钠能与乙酸发生反应产生乙酸钠、二氧化碳和水,又可以溶解丁醇,减少丁醇的气味,还可以降低乙酸丁酯
本题难度:一般