微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有________晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③_______;④加入盐酸调pH;⑤加入__________;⑥过滤;⑦灼烧,冷却,称重。
(3)上述步骤②中所加入的试剂为_____________、____________。
(4)上述步骤④中加盐酸调pH的目的是________________________。
参考答案:(6分)每空1分(1)(NH4)2CO3? (2)过滤;NH
本题解析:
试题分析:(1)二氧化碳通入氨水的过程中,由于开始氨水是过量的,则先有(NH4)2CO3析出。
(2)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,将生成的碳酸钙和氢氧化镁沉淀过滤后除去,然后加入盐酸酸化,以及除去过量的碳酸钠。最后在滤液中加入碳酸氢铵,生成碳酸氢钠和氯化铵。将过滤后得到的碳酸氢钠加热分解即生成碳酸钠。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
2、选择题 下列对有关化学反应过程或实验现象的解释中,正确的是( ???)
A.Cl2的水溶液可以导电,说明Cl2是电解质
B.在少量Fe(NO3)2试样的水溶液中,滴加稀H2SO4酸化,再滴加KSCN溶液变成血红色,说明Fe(NO3)2试样已经变质
C.向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2
D.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后,溶液褪色,说明BaCl2溶液有酸性
参考答案:C
本题解析:略
本题难度:简单
3、实验题 (12分)目前市场销售的某种食用精制盐包装袋上有如下说明:
产品标准
| GB5461
|
产品等级
| 一级
|
配料
| 食盐、碘酸钾、抗结剂
|
碘含量(以I计)
| 20~50mg/kg
|
分装日期
| ?
|
分装企业
| ?
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
???KIO3+???KI+???H2SO4=???K2SO4+???I2+???H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是?????????????????????????????。
②某学生设计回收四氯化碳的操作步骤为:
a?将碘的四氯化碳溶液置于分液漏斗中;
b?加入适量;
c?分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是??????????????????????。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a?准确称取wg食盐,加适量蒸馏水使其完全溶解;
b?用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c?以淀粉为指示剂,逐滴加入物质的量浓度为1.00×10-3mol・L-1的Na2S2O3溶液24.00mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是?????????????????????。
②b中反应所产生的I2的物质的量是?????????mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)????mg/kg。
参考答案:(1)1、5、3、3、3、3
(2)①I2+SO32-
本题解析:
试题分析:(1)根据化合价升降法配平方程式为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(2)①Na2SO3溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+。
②回收CCl4的时候,加入Na2SO3溶液后,要振荡静置,然后才能分液,所以在步骤b后,增加操作:将分液漏斗充分振荡后静置。
(3)①以淀粉做指示剂的时候,当I2反应完后,恰好完全反应,所以溶液由蓝色变为无色。
②反应后生成I2的物质的量为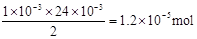 。 。
精制盐的含碘量为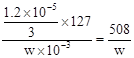
点评:本题很基础,主要考查学生的计算能力和分析问题的能力。
本题难度:一般
4、选择题 下列实验操作中错误的是?????????????????????????????????????????????
A.过滤时玻璃棒末端轻轻地靠在三层滤纸上
B.蒸馏时冷凝水从冷凝管下口进上口出
C.分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:D
本题解析:略
本题难度:简单
5、实验题 (6分)某实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
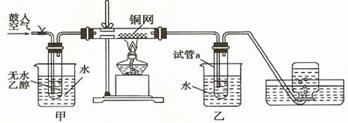
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式___________________。
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应
是???????反应。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有???????????????。要除去该物质,可在混合液中加入????????(填写字母)。
A.氯化钠溶液
B.苯
C.碳酸氢钠溶液
D.四氯化碳
然后,再通过???????(填实验操作名称)即可除去。
参考答案:(1)2Cu+O2 本题解析:考查乙醇催化氧化原理 本题解析:考查乙醇催化氧化原理
(1)红色是铜的颜色,黑色是氧化铜的颜色。说明在加热的条件下铜被空气氧化生成氧化铜,氧化铜在加热的条件下又被乙醇还原生成了铜。
(2)熄灭酒精灯后,反应仍然能进行,说明反应是放热反应,放出的热量足以维持反应的进行。
(3)试纸显红色,说明溶液显酸性,这说明在反应过程中有乙酸生成,所以要除去乙酸,可以用碳酸氢钠溶液即可。由于乙醛的沸点比较低,通过蒸馏即可。
本题难度:一般
|