微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某原电池总反应的离子方程式为2Fe3++Fe==3Fe2+,能实现该反应的原电池是[???? ]
A.正极为铜,负极为铁,电解质溶液为FeCl3溶液
B.正极为铜,负极为铁,电解质溶液为Fe(NO3)2溶液
C.正极为铁,负极为锌,电解质溶液为Fe2(SO4)3溶液
D.正极为银,负极为铁,电解质溶液为CuSO4溶液
参考答案:A
本题解析:
本题难度:简单
2、填空题 (8分)由A、B、C、D四种金属按下表中装置进行实验。
装置
| (Ⅰ)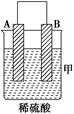
| (Ⅱ)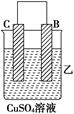
| (Ⅲ)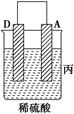
|
现象
| 二价金属A不断溶解
| C的质量增加
| A上有气体产生
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活泼性由强到弱的顺序是________。
参考答案:(1)A-2e-===A2+ (2)Cu2++2e-==="
本题解析:
试题分析:(1)二价金属A不断溶解,这说明A电极是负极,所以电极反应式是A-2e-===A2+。
(2)C的质量增加,上面C电极是正极,溶液中的铜离子放电析出铜单质,所以正极反应式是Cu2++2e-===Cu。
(3)A上有气体产生,所以A是原电池的正极,溶液中的氢离子放电,因此溶液的pH增大。
(4)由于在原电池中,较活泼的金属作负极,不活泼的金属作正极。因此四种金属活泼性由强到弱的顺序是D>A>B>C。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经
本题难度:一般
3、选择题 下图是氢氧燃料电池构造示意图。下列说法不正确的是
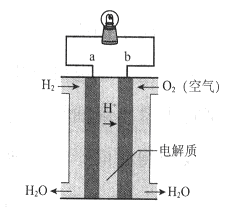
A.a极是负极
B.电子由b通过灯泡流向a
C.该电池总反应是2H2+ O2= 2H2O
D.该装置可将化学能转化为电能
参考答案:B
本题解析:
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。因此在氢氧燃料电池中,氢气在负极通入,氧气在正极通入,则a电极是负极,b电极是正极,A正确;电子由a通过灯泡流向b,B不正确;该电池的正反应就是氢气和氧气反应生成水,即2H2+ O2=2H2O,C正确;原电池是把化学能转化为电能的装置,D正确,答案选B。
点评:该题是基础性试题的考查,难度不大。明确原电池的工作原理是答题的关键,注意电极名称和电极反应式
本题难度:一般
4、选择题 实验中欲制得H2,最好的方法是
A.纯锌与稀H2SO4
B.纯锌和浓H2SO4
C.纯锌与稀盐酸
D.粗锌(含铜杂质)与稀H2SO4
参考答案:D
本题解析:铜、锌、稀H2SO4形成原电池.原电池反应可加快化学反应速率.
本题难度:一般
5、填空题 (14分)磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:①SO2 (g) +Cl2 (g)+ SCl2 (g) 2SOCl2 (g) △H="a" kJ・mol-1 2SOCl2 (g) △H="a" kJ・mol-1
②SO2Cl2(g)+ SCl2 (g)  2SOCl2(g) △H="b" kJ・mol-1 2SOCl2(g) △H="b" kJ・mol-1
则反应:SO2(g) + Cl2(g) SO2Cl2(g) △H = kJ・mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。 SO2Cl2(g) △H = kJ・mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。
(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5 + 10SO2↑,若生成1molSO2,则转移电子的物质的量为 mol。
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。 SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。
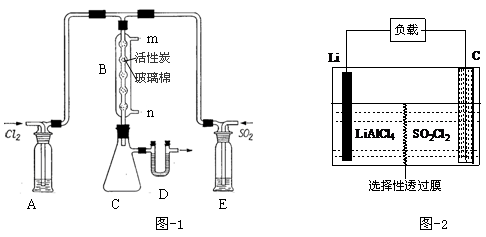
①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为 。
②有关图-1所示的装置说法正确的是 (不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为 。
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如图-2所示,已知电池反应为:2Li + SO2Cl2 =" 2LiCl" + SO2↑;则电池工作时,正极的电极反应式为 。
参考答案:(1)a-b (2分); c(SO2Cl2)/[
本题解析:
试题分析:①-②,整理可得:SO2(g) + Cl2(g)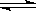 SO2Cl2(g) △H =(a-b)kJ/mol;根据平衡常数的定义可得:该反应平衡常数表达式为K = c(SO2Cl2)/[c(SO2)・c(Cl2)];(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5 + 10SO2↑,根据方程式可知每产生10mol的SO2,转移电子的物质的量是20mol,所以若生成1molSO2,则转移电子的物质的量为2mol。(3)①用浓盐酸与二氧化锰为原料制取Cl2的化学方程式为MnO2 +4HCl(浓) SO2Cl2(g) △H =(a-b)kJ/mol;根据平衡常数的定义可得:该反应平衡常数表达式为K = c(SO2Cl2)/[c(SO2)・c(Cl2)];(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5 + 10SO2↑,根据方程式可知每产生10mol的SO2,转移电子的物质的量是20mol,所以若生成1molSO2,则转移电子的物质的量为2mol。(3)①用浓盐酸与二氧化锰为原料制取Cl2的化学方程式为MnO2 +4HCl(浓) 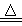 MnCl2 + Cl2↑ +2H2O;a.潮湿的氯气与SO2会发生反应产生盐酸和硫酸,所以A、E处洗气瓶中盛放的不可能分别是饱和食盐水和饱和NaHSO3溶液,错误;b.B处反应管内五球中玻璃棉上的活性炭作催化剂,正确;c.为了是冷凝效果增强,在B处反应管冷却水应从n接口通入,错误;d.因为SO2(g)+ Cl2(g) MnCl2 + Cl2↑ +2H2O;a.潮湿的氯气与SO2会发生反应产生盐酸和硫酸,所以A、E处洗气瓶中盛放的不可能分别是饱和食盐水和饱和NaHSO3溶液,错误;b.B处反应管内五球中玻璃棉上的活性炭作催化剂,正确;c.为了是冷凝效果增强,在B处反应管冷却水应从n接口通入,错误;d.因为SO2(g)+ Cl2(g)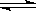 SO2Cl2(g) 的反应是放热反应,所以根据平衡移动原理,应该降低温度,所以装置C处吸滤瓶应放在冰水中冷却才可以提高SO2Cl2的产率;e.由于SO2、Cl2都是大气污染物,因此在排放之前应该进行尾气处理,二者都可以与碱性物质发生反应,所以在D处U形管中盛放的可能是碱石灰,正确。③从化学平衡移动角度分析,反应管通水冷却的目的为冷凝、降温均有利于SO2Cl2生成;(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如题20图-2所示,已知电池反应为:2Li + SO2Cl2 =" 2LiCl" + SO2↑;则电池工作时,在正极上发生还原反应,该电极反应式为SO2Cl2 + 2e- = 2Cl-+ SO2↑。 SO2Cl2(g) 的反应是放热反应,所以根据平衡移动原理,应该降低温度,所以装置C处吸滤瓶应放在冰水中冷却才可以提高SO2Cl2的产率;e.由于SO2、Cl2都是大气污染物,因此在排放之前应该进行尾气处理,二者都可以与碱性物质发生反应,所以在D处U形管中盛放的可能是碱石灰,正确。③从化学平衡移动角度分析,反应管通水冷却的目的为冷凝、降温均有利于SO2Cl2生成;(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如题20图-2所示,已知电池反应为:2Li + SO2Cl2 =" 2LiCl" + SO2↑;则电池工作时,在正极上发生还原反应,该电极反应式为SO2Cl2 + 2e- = 2Cl-+ SO2↑。
考点:考查盖斯定律的应用、氯气的实验室正确方法的方程式表示、反应条件的控制、原电池反应原理的知识。
本题难度:困难
|