微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某化学反应2A(g) B(g)+D(g)在密闭容器中分别在下列四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol・L-1)随反应时间(min)的变化情况如下表:
B(g)+D(g)在密闭容器中分别在下列四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol・L-1)随反应时间(min)的变化情况如下表:
实验序号?时间
| 0
| 2
| 3
| 4
|
800
| ℃
| 800
| ℃
|
1
| 1.0
| c2
| c3
| 1.0
|
10
| 0.80
| 0.60
| 0.92
| 0.20
|
20
| 0.67
| 0.50
| 0.75
| 0.20
|
30
| 0.57
| 0.50
| 0.63
| 0.20
|
40
| 0.50
| 0.50
| 0.60
| 0.20
|
50
| 0.50
| 0.50
| 0.60
| 0.20
|
60
| 0.50
| 0.50
| 0.60
| 0.20
|
(1)实验1中,反应在10至20分钟内平均化学反应速率为v(A)=______________。
(2)实验2中,A的初始浓度c2=______________mol・L-1,反应经20 min就达到平衡,可推测实验2中隐含的条件可能是_______________。
(3)若实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3______________v1(填“<”“>”或“=”=,且c3______________(填“<”“>”或“=”=1.0 mol・L-1。
(4)比较实验4和实验1,可推测该反应的正反应是______________(填“吸热”或“放热”反应)。理由是__________________________________________________________________。
参考答案:(1)0.013 mol・L-1・min-1
(2)1
本题解析:(1)v(A)=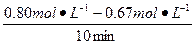 ="0.013" mol・L-1・min-1
="0.013" mol・L-1・min-1
(2)对比实验2与实验1,可知从10 min到20 min,实验1中A的浓度相同,说明是同一平衡状态,即c2="1.0" mol・L-1。又因实际反应的速率快,达平衡所需的时间短,说明反应中使用了催化剂。
(3)对比实验3与实验1,可知从
本题难度:简单
2、选择题 在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度 ②升高温度 ③移去生成物 ④增大压强 ⑤加入催化剂.
A.①③
B.②④
C.②⑤
D.①⑤
参考答案:增大反应物的浓度和增大压强,只能增大活化分子数,不能增大活化
本题解析:
本题难度:简单
3、填空题 下表是稀硫酸与某金属反应的实验数据:
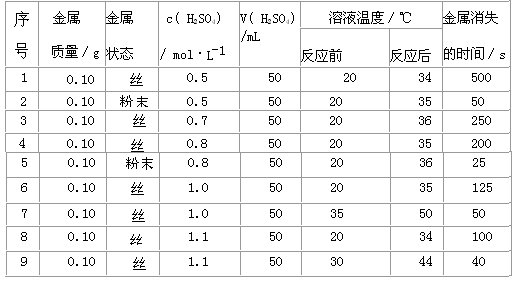
分析上述数据,回答下列问题:
(1)实验4和5表明,___________对反应速率有影响,________反应速率越快,能表明同一规律的实验还有________________________________ (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有_____________(填实验序号);
(3)本实验中影响反应速率的其他因素还有____________,其实验序号是___________
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:_____________________________________________________ 。
参考答案:(1)固体反应物的表面积;表面积越大;l和2?
(2)
本题解析:
本题难度:一般
4、选择题 在生活、生产中为增大反应速率而采取的措施合理的是
A.食物放在冰箱中
B.塑料制品中添加抑制剂
C.在糕点包装内放置小包除氧剂
D.燃煤发电时用煤粉代替煤块
参考答案:D
本题解析:
试题分析:A、冰箱内温度低,反应速率减慢,食物存放时间长,错误;B、塑料制品中添加抑制剂,减慢塑料的老化,错误;C、在糕点包装内放置小包除氧剂,防止糕点被氧化变质,错误;D、燃煤发电时用煤粉代替煤块,增大煤与氧气的接触面积,反应速率加快,正确,答案选D。
本题难度:简单
5、计算题 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下的方案。
编号
| H2C2O4溶液
| 酸性KMnO4溶液
| 温度/℃
|
浓度/ mol?L-1
| 体积/mL
| 浓度/ mol?L-1
| 体积/mL
|
①
| 0.10
| 2.0
| 0.010
| 4.0
| 25
|
②
| 0.20
| 2.0
| 0.010
| 4.0
| 25
|
③
| 0.20
| 2.0
| 0.010
| 4.0
| 50
?
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,每消耗1mol H2C2O4转移_____mol 电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:c(H2C2O4)∶c(KMnO4) ≥______________。
(2)探究温度对化学反应速率影响的实验编号是___________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是_____________。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______________ mol?L-1?min-1。
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图。若保持其他条件不变,请在答题卡坐标图中,画出25℃时c(MnO4-)~t的变化曲线示意图。

参考答案:(16分)(1)2??? 2.5(每空3分)
(2)②
本题解析:
试题分析:(1)草酸中碳元素为+3价,二氧化碳中碳元素为+4价,由化合价升高总数等于转移电子数可知1个H2C2O4转移2个电子,则每消耗1molH2C2O4转移2mol 电子;草酸与酸性高锰酸钾溶液反应为5H2C2O4+2KMnO4+3H2SO4=10CO2↑+K2SO4+2MnSO4+8H2O~10e-,只有当KMnO4完全反应,溶液的紫红色才能褪去,如果n(H2C2O4)=5mol、n(KMnO4)≤2mol,就能观察到紫色褪去,所以c(H2C2O4)∶c(KMnO4) = n(H2C2O4)
本题难度:困难
|