微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 FeCl3可用作印刷电路铜板腐蚀剂。为回收废腐蚀液中的铜,必须对废腐蚀液的组成进行分析。某同学取废腐蚀液200 mL,分成甲、乙两等份。向甲溶液中滴加AgNO3溶液至不再有沉淀产生,得到沉淀129.15 g;向乙溶液中加入10 g足量铁粉,充分反应,剩余固体质量4.8 g。计算中忽略溶液体积的变化。
(1)废腐蚀液中Cl-的物质的量浓度是________。
(2)废腐蚀液中Cu2+的物质的量浓度是________。
参考答案:(1)9 mol/L (2)0.5 mol/L
本题解析:(1)n(Cl-)=n(AgCl)=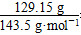 =0.9 mol,c(Cl-)=0.9/0.1=9 mol/L。
=0.9 mol,c(Cl-)=0.9/0.1=9 mol/L。
(2)在FeCl3与Cu反应后的废液中含有FeCl3、FeCl2和CuCl2,向其中加入过量Fe,最终溶液中的溶质是FeCl2,从整个反应过程看,相当于FeCl3与Fe反应生成FeCl2。n(Cu)×64 g/mol+10 g-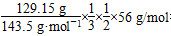 =4.8 g,则n(Cu)=0.05 mol,n(Cu2+)=n(Cu)=0.05 mol。c(Cu2+)=0.05 mol÷0.1 L=0.5 mol/L。
=4.8 g,则n(Cu)=0.05 mol,n(Cu2+)=n(Cu)=0.05 mol。c(Cu2+)=0.05 mol÷0.1 L=0.5 mol/L。
本题难度:一般
2、选择题 某原子的摩尔质量是M g?mol-1,则一个该原子的真实质量约是(???)???????????????
A.M g
B.1/M g
C.M/6.02×1023g
D.6.02×1023/M g
参考答案:C
本题解析:略
本题难度:简单
3、选择题 下列叙述正确的是
A.1 mol CH4的质量为16g/mol
B.H2O的摩尔质量为18 g
C.44 g CO2的体积为22.4 L
D.9.8 g H2SO4含0.1NA个H2SO4分子
参考答案:D
本题解析:A错误,质量的单位不是g/mol。
B错误,摩尔质量的单位是g/mol。
C错误,因为不知道气体所处的状态是不是标况。
D正确。
本题难度:一般
4、选择题 同温、同压下,X g的甲气体和Y g乙气体占有相同的体积,则X∶Y的值可以表示为(???)
A.甲与乙的相对分子质量之比
B.等质量的甲与乙的分子个数之比
C.同温、同压下甲与乙的密度之比
D.等质量的甲与乙的原子个数之比
参考答案:AC
本题解析:根据阿伏加德罗定律,同温、同压、同体积,则甲、乙两气体含有相同数目或相同物质的量的分子,则X∶Y为两者的摩尔质量之比。由此推出A、C正确。
本题难度:简单
5、选择题 用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A.常温常压下,6g H2O中含有的原子数目为NA
B.标准状况下,22.4LCO2含有的分子数目为NA
C.1L1mol・L-1K2SO4溶液中含有的钾离子数目为NA
D.常温常压下,11.2 L氯气与足量铜粉充分反应,转移的电子数为NA
参考答案:AB
本题解析:
试题分析:C项1L1mol・L-1K2SO4溶液中含有的钾离子数目应该为2NA,错误;D项由于不在标准状况下,无法计算,错误。
本题难度:一般