微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式________________。
(2)根据等电子原理,写出CO分子结构式_________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
?①甲醇的沸点比甲醛的高,其主要原因是_______________________;甲醛分子中碳原子轨道的杂化类型为_____________。
②甲醛分子的空间构型是_______________;1mol甲醛分子中σ键的数目为__________________。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为__________________。
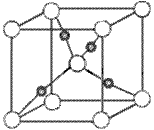
参考答案:(1)![]() 本题解析:
本题解析:
本题难度:一般
2、选择题 某原子核外共有6个电子,分布在K与L电子层上,在下列L层分布中正确的是[???? ]
A.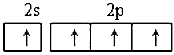
B.
C.
D.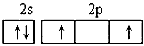
参考答案:D
本题解析:
本题难度:简单
3、选择题 有关甲醛分子(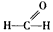 )的说法正确的是[???? ]
)的说法正确的是[???? ]
A.C原子采取sp杂化
B.甲醛分子为三角锥形结构
C.C原子采取sp2杂化
D.甲醛分子为平面三角形结构
参考答案:CD
本题解析:
本题难度:简单
4、简答题 (1)氨分子中氮原子采用sp3杂化,可为什么氨分子为三角锥形,键角是107°?
________________________________
(2)为什么H2O分子的键角既不是90° 也不是109°28’,而是105°?
________________________________
参考答案:(1)sp3杂化轨道分别指向正四面体的4个顶点,4个轨道的对
本题解析:
本题难度:一般
5、选择题 下列物质的化学用语正确的是( )
A.NH4H的电子式:
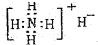
B.硝基苯的结构简式:

C.甲烷分子的比例模型:
D.sp2杂化轨道模型:

参考答案:D
本题解析:
本题难度:简单