��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����£������й�������ȷ���ǣ�������
A��NaB��Һ��pH=8��c��Na+��-c��B-��=9.9��10-7mol?L-1
B��Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3��
C��pH��ȵĢ�NH4C1���ڣ�NH4��2SO4����NH4HSO4������Һ�У�c��NH4+����С˳��Ϊ����=�ڣ���
D��10mLpH=12������������Һ�м���pH=2��HA��pH�պõ���7��������Һ���V?���ܣ�=20mL����������ˮ���
2������� ��֪��CO2+3H2O+2AlO2-�T2Al��OH��3��+CO32-������Ũ��Ϊ0.1mol?L-1�����ֵ������Һ����Na2CO3???��NaHCO3��NaAlO2��CH3COONa??��NaOH
��1����������Һ��pH��С�����˳����______�����ţ���
��2����������Һϡ����ͬ�ı���ʱ����pH�仯������______�����ţ���
��3�����̼�ᣨH2CO3����Һ��NaAlO2��Һ����д�����ܷ����Ļ�ѧ��Ӧ����ʽ��______��
��4�������£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
| ʵ���� | HA���ʵ���Ũ�ȣ�mol/L�� | NaOH���ʵ���Ũ�ȣ�mol/L�� | �����Һ��pH
��
0.20
0.20
pH=a
��
0.10
0.10
pH=8.00
�����������ʵ���������Ӽ�����������������a�������Һ��pH����˵��HA��ǿ�ỹ������______��
����ʵ�����û����Һ����ˮ�������c?��OH-��=______mol/L��
����û����Һ��������ʽ��ֵ��
I��c?��Na+��-c?��A-��=______��
II��c?��OH-��-c?��HA��=______��
3��ѡ���� ��֪��H2B��ˮ��Һ�д������й�ϵ����H2B = H+ + HB������HB��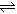 H+ + B2�� ��������˵����һ������ȷ����[???? ] H+ + B2�� ��������˵����һ������ȷ����[???? ]
A��NaHB��Һһ�������ԣ�Na2B��Һһ���ʼ���
B����Na2B��Һ��һ���У�c (Na+)=2(c (B2��)+c (HB��) + c (H2B) )
C��NaHBˮ��Һ��һ���У�c (Na+) + c (H+) =c (HB��) + c (OH��) +2 c (B2��)
D����Na2B��Һ��һ���У� c (OH��)=c (H+) + c (HB��)
4������� ����Ũ�Ⱦ�Ϊ0.1mol?L-1��������Һ��
�����ᡢ�ڴ��ᡢ���������ơ����Ȼ�李��ݴ���李���������李��߰�ˮ��
��ش��������⣺
��1���١��ڡ��ۡ���������Һ����ˮ�������H+Ũ���ɴ�С��˳���ǣ�����ţ�______��
��2���ܡ��ݡ��ޡ���������Һ��NH4+Ũ���ɴ�С��˳���ǣ�����ţ�______��
��3�����ۺܰ͢������1��2��Ϻ��Һ�и�����Ũ���ɴ�С��˳����______��
��4����֪t��ʱ��KW=1��10-13����t�棨���������������=����______25�森��t��ʱ��pH=11��NaOH��ҺaL��pH=1��H2SO4��ҺbL��ϣ����Ի�Ϻ���Һ����ı仯���������û����Һ��pH=2����a��b=______��
��5��ͬ�����ͬ���ʵ���Ũ�ȵĢ�����͢ڴ�����Һ���ֱ���ͬŨ�ȵ�NaOH��Һ��ȫ�кͣ�����NaOH�����С��ϵΪ��______�ڣ����������������=������
��6��ͬ�������ͬPH�Ģ�����͢ڴ�����Һ�зֱ�Ͷ�������ҵ�������п����ʼ��H2�����ʣ���______�ڣ�Ƭ�̺��______�ڣ�����Ӧ����������ʱ���______�ڣ�
5��ѡ���� �����ΪVa��0.05 mol/L CH3COOH��Һ�м������ΪVb��0.05 mol/L KOH��Һ�����й�ϵ�������[???? ]
A��Va>Vbʱ��c(CH3COOH) +c(CH3COO-)>c(K+)
B��Va=Vbʱ��c(CH3COOH)+c(H+)=c(OH-)
C��Va<Vbʱ��c(CH3COO-)>c(K+)c(OH-)>c(H+)?
D��Va��Vb�������ʱ��c(K+) +c(H+) =c(OH-)+c(CH3COO-)
|