微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol・L-1 HNO3、2.00 mol・L-1 HNO3,细颗粒大理石、粗颗粒大理石,35 ℃水浴。
(1)他们能完成哪些因素对速率影响的探究?
____________________________________________________________。
(2)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:

(3)整个实验中应控制的不变量是硝酸溶液体积和????????????????。
(4)该实验小组用如图实验装置进行实验。
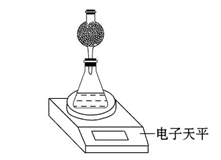
①除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有???????。
②干燥管中应放置的试剂是??????????????。
A.碱石灰
B.无水CaCl2
C.P2O5固体
D.浓硫酸
③若撤除干燥管装置,所测速率???????????(填“偏大”、“偏小”或“不变”)。
参考答案:(1)硝酸浓度、温度、大理石表面积
(2)
实验
本题解析:解答本题时应注意以下三点:
(1)根据所给数据分析影响反应速率的因素。
(2)分析外界因素对反应速率的影响时,要采取变量控制的方法,控制只有一个因素发生变化,其他因素不变。
(3)考虑减小误差所采取的措施。
(1)根据所给的试剂可知有两种不同浓度的硝酸,因此可比较浓度对反应速率的影响;有两种不同状态的大理石,因此可比较固体表面积对反应速率的影响;还有35 ℃水浴,因此可比较温度对反应速率的影响。
(2)因为①与②的不同是HNO3浓度不同,所以其他的因素应该相同。若①中大理石为
本题难度:一般
2、实验题 (8分)在锌与盐酸反应的实验中,某学生得到的结果如下表所示:

(1)t1= s。
(2)根据表中数据得出关于温度影响反应速率的结论是 。
(3)t1 t4(填“>”、“<”、“=”),原因是  。
。
(4)t2 t3(填“>”、“<”、“=”),原因是 。
参考答案:
 本题解析:略
本题解析:略
本题难度:一般
3、选择题 下列条件不能使反应:N2+3H2?
催化剂
高温高压
2NH3的正反应速率加快的是( )
A.?增大N2浓度
B.?升高温度
C.?增大压强
D.?减小NH3浓度
参考答案:A、增大反应物氮气的浓度,活化分子的数目增多,正、逆反应速率
本题解析:
本题难度:简单
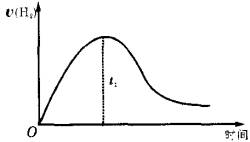
4、填空题 下图为将Zn投入一定浓度体积的H2SO4中,解释图像的成因(纵坐标为H2的生成速率)
参考答案:详见解析
本题解析:由图像可知氢气的生成速率随时间先后由慢到快,然后又由快到慢,反应体系中硫酸所提供的氢离于浓度由大到小。若氢气的生成速率由其决定,速率的变化趋势也应由快到慢,反应前半程的原因只能是温度所致,锌与硫酸反应时放热,体系温度逐渐升高,温度对反应速率的影响占主导地位,一定时间后,硫酸的浓度下降占据主导地位,因而氢气的生成速率随时间先由慢到快,然后又由快到慢。
本题难度:简单
5、选择题 用锌粒与稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是( )
A.升高反应体系的温度
B.增加锌粒的用量
C.不用锌粒,改用锌粉
D.加入少量浓硫酸
参考答案:A、升高反应体系的温度,反应速率加快,故A不选;
B、
本题解析:
本题难度:一般