微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 应2X(g)+Y(g) 2Z(g);△H<0(正反应为放热反应) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
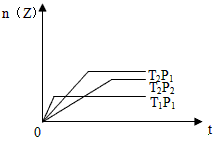
[ ??? ]
A.T1<T2,P1<P2
B.T1<T2,P1>P2
C.T1>T2,P1>P2
D.T1>T2,P1<P2
2、填空题 (本题8分)汽车尾气是造成雾霾天气的重要原因之一。已知:
①N2(g)+O2(g) 2NO(g) ΔH1 ②2NO(g)+O2(g)
2NO(g) ΔH1 ②2NO(g)+O2(g) 2NO2(g) ΔH2
2NO2(g) ΔH2
③CO2(g) CO(g)+1/2O2(g) ΔH3 ④2CO(g)+2NO(g)
CO(g)+1/2O2(g) ΔH3 ④2CO(g)+2NO(g) N2(g)+2CO2(g) ΔH4
N2(g)+2CO2(g) ΔH4
请完成以下问题:
(1)请根据反应①②③,确定反应④中ΔH4= 。
(2)根据图1,反应④的热化学方程式为: 。
该反应在 (填“高温”“低温”或“任意温度”)下有利于该反应正向自发。
(3)图2表示反应④的反应物NO、CO的起始物质的量比、温度对平衡时CO2的体积分数的影响。
①W、Y、Z三点的平衡常数的大小关系为: , X、Y、Z三点,CO的转化率由大到小的顺序是 。
②T1℃时,在1L密闭容器中,0.1molCO和0.1molNO,达到Y点时,测得NO的浓度为0.02mol/L,则此温度下平衡常数K= (算出数值)。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01 mol/L、a mol/L、0.01 mol/L、0.04 mol/L,要使反应向正方向进行,a的取值范围为 。

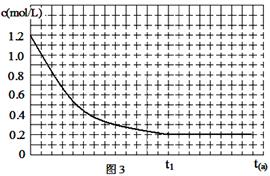
(4)恒温恒容时,反应④中NO、CO按一定比例投料,反应过程中CO浓度随时间的变化关系如图3所示,请在同一图中绘出N2浓度随时间的变化曲线。
3、选择题 对于平衡体系mA(g)+nB(g)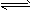 pC(g)+qD(g);△H<0 。下列结论中不正确的是 [???? ]
pC(g)+qD(g);△H<0 。下列结论中不正确的是 [???? ]
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为 m : n
C.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
D.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol
4、填空题 氮及其化合物与我们的吃、穿、住、行、健康等都有着密切的联系,也是高中化学学习中重要的一部分。请回答下列问题:
(1)一定条件下,向一个2L的密闭容器中充入2mol N2和6 molH2,反应达平衡时放出93 kJ热量,生成NH3
的浓度为1mol/L,试写出该反应的热化学方程式:______________________
(2)现有一支10 mL的试管,充满NO倒置于水槽中,向试管中缓缓通入一定量氧气,当试管内液面稳定时,剩余气体2 mL。则通入氧气的体积可能为__________________
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)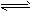 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
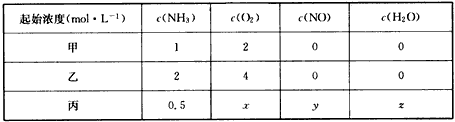
①恒温恒容下,平衡时NH3的转化率甲____(填“>”“=”或“<”)乙。
②恒温恒容下,若要使丙与甲平衡时各组分浓度相同,则x=____,y=____,z=____。
(4)向容积相同、温度分别为T1和T2的两个密闭容器中分别充入等量NO2,发生反应:
2NO2(g)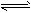 N2O4(g) △H<0。恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和
N2O4(g) △H<0。恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和
a2。已知T1<T2,则a1____a2。
A.大于 B.小于 C.等于 D.以上都有可能
(5)标准状况下,将干燥纯净的氨和二氧化氮气体分别完成喷泉实验后所得溶液等体积混合,反应后溶液中的离子浓度关系正确的是____。
A.c(NO3-)>c(NH4+)>c(H+)>c(OH-)
B.c(NH4+)>c(NO3-)>c(OH-)>c(H+)
C.c(H+)=c(OH-)+c(NH3・H2O)
D.c(NH4+)+c(NH3・H2O)=1.5c(NO3-)
5、填空题 (6分)(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) CO2(g)十H2 (g),△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)= mol/(L・min),此时该反应的平衡常数为 。
CO2(g)十H2 (g),△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)= mol/(L・min),此时该反应的平衡常数为 。
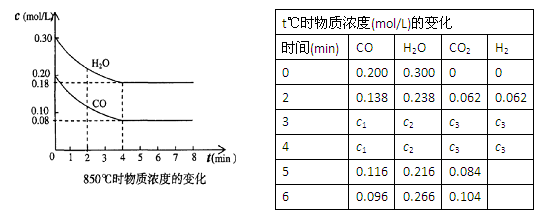
(2)T ℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于  状态;c1 0.08 (填 “>”、“<”或“=”)。
状态;c1 0.08 (填 “>”、“<”或“=”)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是 (填序号,下同),表中5min~6min之间数值发生变化,可能的原因是 。
a.增加了水蒸气的量 b.降低温度
c.使用催化剂 d.增加氢气的浓度