微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1?mol氢气中的化学键消耗的能量为Q1kJ,破坏1?mol氯气中的化学键消耗的能量为Q2?kJ,形成1?mol氯化氢中的化学键释放的能量为Q3?kJ。下列关系式正确的是 [???? ]
A.Q1+Q2>Q3????
B.Q1+Q2>?2Q3 ??
C.Q1+QE<Q3????
D.Q1+Q2<2Q3
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列叙述中正确的是
A.分子是由一定数目的原子组成,原子之间相互作用叫化学键
B.阴阳离子通过静电作用所形成的化学键叫做离子键
C.非金属元素间构成的化合物都不是离子化合物
D.离子化 合物中一定会有离子键
参考答案:BD
本题解析:
试题分析:相邻原子或离子之间强烈的相互作用是化学键,A不正确,原子之间的相互作用不一定是化学键;非金属元素间构成的化合物也可以是离子化合物,例如氯化铵等,C这笔钱,BD正确,答案选BD。
点评:该题是中等难度的试题,也是高考中的常见题型和重要的考点,主要是考查学生对化学键含义以及化学键与化合物关系的熟悉了解程度,意在巩固学生的基础,提高学生的能力。有利于培养学生的逻辑推理能力和灵活应变能力。
本题难度:一般
3、填空题 (6分)火箭推进器中 盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol液态 H2O2混合恰好完全反应,生成氮气和水蒸气,放出256 kJ的热量。
(1)反应的热化学方程式为 。
(2)又已知16g液态肼与液态双氧水反应生成液态水时放出的热量是408 kJ。则H2O(g)=H2O(l)
的ΔH= 。
(3)已知N2(g) + 2O2(g) ="=" 2NO2(g);△H=+67.7KJ/mol,
N2H4(g) + O2(g) ="=" N2(g)+2H2O(g);△H= ―534KJ/mol,
则肼与NO2完全反应的热化学方程式为_____ _____________________。
参考答案:(1)反应的热化学方程式为N2H4(g)+2H2O2(l)=
本题解析:
诗题分析:(1)0.4mol液态肼和0.8mol液态 H2O2混合恰好完全反应,生成氮气和水蒸气,放出256 kJ的热量。说明1摩尔液态肼与2摩尔液态过氧化氢反应恰好反应生成氮气和水蒸气,放出640 kJ,所有热方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)ΔH="-640" kJ・mol-1;(2)N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)ΔH="-816" kJ・mol-1,根据盖斯定律分析,H2O(g)=H2O(l)的反应热等于[(-816)-(640)]/2=-44 kJ・mol-1;(3)根据盖斯定律,方程式二×2--方程式一,△H= 2×―534KJ/mol-(+67.7KJ/mol)=―1135.7KJ/mol.
考点:盖斯定律,热化学方程式的书写。
本题难度:一般
4、选择题 已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量 ②1molCl2分子中化学键断裂时需要吸收243kJ的能量 ③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量。 下列叙述正确的是 [???? ]
A.氢气与氯气反应生成2mol氯化氢气体,需要释放183kJ的热量
B.氢气与氯气反应生成2mol氯化氢气体,需要吸收183kJ的热量
C.氢气与氯气反应生成1mol氯化氢气体,需要吸收183kJ的热量
D.氢气与氯气反应生成1mol氯化氢气体,需要释放183kJ的热量
参考答案:A
本题解析:
本题难度:一般
5、选择题 下列热化学方程式书写正确的是( )
A.2SO2+O2 2SO3 ΔH=-196.6 kJ・mol-1
2SO3 ΔH=-196.6 kJ・mol-1
B.H2(g)+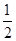 O2(g)===H2O(l)ΔH=-285.8 kJ・mol-1
O2(g)===H2O(l)ΔH=-285.8 kJ・mol-1
C.2H2(g)+O2(g)===2H2O(l) ΔH=+571.6 kJ・mol-1
D.C(s)+O2(g)===CO2(g)ΔH=393.5 kJ・mol-1
参考答案:B
本题解析:考查热化学方程式的正误判断。热化学方程式是表示化学反应与反应热关系的方程式。书写和应用热化学方程式时必须注意以下几点:
①明确写出反应的计量方程式,各物质化学式前的化学计量系数可以是整数,也可以是分数。
②各物质化学式右侧用圆括弧()表明物质的聚集状态。可以用g、l、s分别代表气态、液态、固态。固体有不同晶态时,还需将晶态注明,例如S(斜方),S(单斜),C(石墨),C(金刚石)等。溶液中的反应物质,则须注明其浓度,以aq代表水溶液,(aq) 代表无限稀释水溶液。
③反应热与反应方程式相互对应。若反应式的书写形式不同,则相应的化学计量系数不同,故反应热亦不同。
④热化学方程式必须标明反应的浓度、温度和压力等条件,若在常温常压时可省略。所以只有选项B是正确的,其余都是错误的,答案选B。
本题难度:一般