微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变化,则下列叙述正确的是
 [???? ]
[???? ]
A.在①中Cu棒为阳极;在②中Cu棒为负极
B.电极上析出物质的质量:①<②
C.电极反应式:①中阳极:4OH-一4e-= 2H2O+O2↑;②中负极:2H+ + 2e- = H2↑
D.溶液的pH:①不变;②增大
参考答案:D
本题解析:
本题难度:一般
2、选择题 用惰性电极电解下列各组中的三种电解质稀溶液,在电解的过程中,溶液的PH依次为升高、降低、不变的是( )
A.AgNO3CuCl2Cu(NO3)2
B.KBrNa2SO4CuSO4
C.CaCl2KOHNaNO3
D.HClHNO3K2SO4
参考答案:A、电解AgNO3会生成硝酸、银和氧气,电解CuCl2会生成
本题解析:
本题难度:一般
3、选择题 铅蓄电池的工作原理为Pb + PbO2 + 4H+ + 2SO42-?==?2PbSO4 + 2H2O。研读上图,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极。先闭合K1足够长时间后断开K1。下列有关说法中不正确的是:

A.1mol Pb和1mol PbO2具有的总能量大于2mol PbSO4具有的总能量
B.若将两U形管中的溶液混合,混合液的质量分数仍为30%
C.两U型管均可单独作为原电池使用,正极分别为A和F
D.若再单独闭合K2,电极A、B的质量会逐渐增加,电极E、F的质量会逐渐减小
参考答案:A
本题解析:
答案:A
A、不正确,1mol Pb、1mol PbO2和2molH2SO4具有的总能量大于2mol PbSO4和2molH2O具有的总能量。B、正确,生成的硫酸和反应的硫酸质量相同;C、D正确;
本题难度:一般
4、简答题 据最近新闻报道,我国200多个城市的地下水,超过一半受到污染.某城市地下水中,主要含钙离子、镁离子、氯离子和硫酸根离子.请思考下列问题:
(1)该水属于______硬水(填写“暂时”或“永久”).目前常用阴、阳离子交换树脂来进行水的软化,当阴离子交换树脂失效后可放入______溶液中再生.
(2)国际上提出了“预防污染”这一新概念,绿色化学是“预防污染”的基本手段,下列各项中有关水的实施措施中,属于“预防污染”这一新概念的是______
?A.节约用水???? B.处罚废水排放不达标企业??? C.将污水注入地下深井??? D.杜绝污染源
(3)海水淡化可以也获得生活用淡水.下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、
SO
?
2-4
等离子,电极为惰性电极.请分析下列问题:
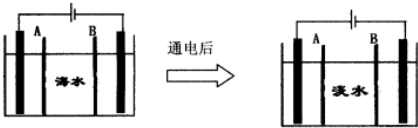
①在A、B两个交换膜中,属于阳离子交换膜是______(填字母标号).
②写出通电后阳极的电极反应式:______.
参考答案:(1)因水的硬度是由钙和镁的硫酸盐或氯化物等引起的,这种硬度
本题解析:
本题难度:一般
5、实验题 (18分)废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备CoxOy,的工艺流程简图如下:

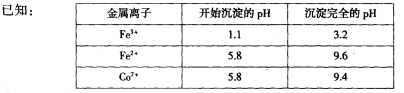
(1)电解时废旧刀具作阳极,不锈钢作阴极,盐酸的作用是______。
(2)通人氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择pH最大范围是____________。
(3)实验测得NH4HCO3溶液显碱性,制备CoCO3时,选用的加料方式是_______(填代号),原因是_______。
a.将滤液与NH4HCO3溶液同时加入到反应容器中
b.将滤液缓慢加入到盛有NH4HCO3溶液的反应容器中
c.将NH4HCO3溶液缓慢加入到盛有滤液的反应容器中
写出生成CoCO3的离子方程式______________________________________。
(4)实验中获得的若洗涤不充分,在焙烧时会产生污染性气体,该污染性气体的成分为_______________(填化学式)。
(5)实验室用下列装置制取 ,并测定其化学式。
,并测定其化学式。
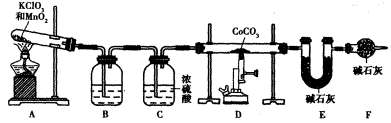
①装置A制得的中含有少量Cl2,则装置B中所盛放的试剂为______(填代号)。
a.NaHCO3溶液??? b.NaOH溶液??? c.KMnO4溶液??? d.饱和NaCI溶液
②在CoCO3完全转化为 后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物
后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物 的化学式为____________。
的化学式为____________。
③若缺少装置F,则导致 的值______(填“偏大”、“偏小”或“无影响”)。
的值______(填“偏大”、“偏小”或“无影响”)。
参考答案:(l)作电解质溶液。(2)3.2≤pH<5.8。
(3
本题解析:
试题分析:由题给工艺流程知,以盐酸为电解质溶液,以废旧刀具作阳极,不锈钢作阴极,进行电解,生成WC,溶液中含有亚铁离子和Co2+,加入双氧水,将亚铁离子氧化为铁离子,通入氨气,调节pH在3.2到5.8之间,将铁离子转化为氢氧化铁沉淀过滤除去,滤液中含有Co2+,加入碳酸氢铵溶液生成碳酸钴,焙烧生成CoxOy。(l)电解时废旧刀具作阳极,不锈钢作阴极,盐酸的作用是作电解质溶液。(2)通人氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择pH最大范围是3.2≤pH<5.8。(3)实
本题难度:一般