��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣�
��1����֪1.505��1023��X������ӵ�����Ϊ8 g�����X��������ʵ���Ϊ ����Ħ������Ϊ ��
��2��n g O2����m��Oԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ
�ο��𰸣�(8��) ��1��0.25mol�� 32g/mol
����������������ʵ������йؼ��㡣
��1������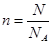 ��֪��1.505��1023��X������ӵ����ʵ�����1.505��1023��6.02��1023/mol��0.25mol������Ϊn��m/M�����Ը������Ħ��������8g��0.25mol��32g/mol��
��֪��1.505��1023��X������ӵ����ʵ�����1.505��1023��6.02��1023/mol��0.25mol������Ϊn��m/M�����Ը������Ħ��������8g��0.25mol��32g/mol��
��2��ng���������ʵ�����n/32mol������Ϊ��������2����ԭ�ӹ��ɵģ����Ը���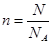 ��֪�������ӵ�����NA����ֵ�ɱ�ʾΪ
��֪�������ӵ�����NA����ֵ�ɱ�ʾΪ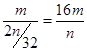 ��
��
�����Ѷȣ�һ��
2��ѡ���� ��NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ�???��
A�������£�23g NO2����NA����ԭ��
B��1 L 0.1mol?L-1�İ�ˮ����0.1NA��OH�D
C����״���£�22.4 L CCl4����NA ��CCl4����
D��1molFe2+��������H2O2��Һ��Ӧ��ת��2NA������
�ο��𰸣�A
���������
���������A��23g NO2 �����ʵ���Ϊ:23g/46g.mol-1="0.5mol," ����ԭ��Ϊ1mol��B��NH3.H2OΪ������ʣ��ʴ���C��CCl4��״���²�������ʴ���D��1molFe2+��������H2O2��Һ��Ӧ��Fe2+��������Fe3+ת��1mol���ӣ��ʴ���
�����Ѷȣ�һ��
3�������� ��4�֣�ͬ��ͬѹ�£�ij��������O2��116 g��������CO2��122 g���ֳ���ij������114 g���������ķ�������
�ο��𰸣���4�֣�28
���������
�����������������������xg��ij�����Ħ��������M�����ݰ���٤�����ɣ�ͬ��ͬѹ�£�ͬ������κ���������ʵ�����ȣ���(116-x)g/32g/mol=(122-x)g/44g/mol�����x=100�����ԣ�116-100��g/32g/mol=(114-100)g/M�����M=28g/mol�����Ը��������Է���������ֵ�ϵ���Ħ����������ֵ�������������Է���������28��
���㣺���鰢��٤�����ɵ�Ӧ�ã���Է��������ļ���
�����Ѷȣ�����
4��ѡ���� ��֪3.0g AO32���к������������������6.02��1022��������˵������ȷ����?
A��Aԭ�ӵ�Ħ������32g/mol����������
B��AO32����Ħ������Ϊ60��
C��3.0gAO32�������ʵ�����0.02mol
D��AԪ�ص����ԭ������Ϊ12
�ο��𰸣�D
���������AO32�� �к������������������2����6.02��1022�����ӵ����ʵ�����0.1mol������3.0g�������ʵ�����0.05mol����Ħ��������3.0g��0.05mo��60g/mol�����Aԭ�ӵ����ԭ��������60��16��3��12����ѡD��
�����Ѷȣ�һ��
5�������� ʹ250 mL�ܶ�Ϊ1.1 g��cm-3����������Ϊ 24.5%���������м��ַ�Ӧ��
(1)���������H2SO4�����ʵ���Ũ�ȣ�
(2)������H2���������״������
(3)�����ɵ������������Ƴ�400 mL��Һ������Һ���������������ʵ���Ũ���Ƕ��٣�
�ο��𰸣�(1)![]() ���������
���������
�����Ѷȣ�һ��