微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为p g/ml,质量分数为W,物质的量浓度为c mol/L,则下列关系中不正确的是( ?? )
A.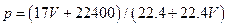
B.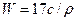
C.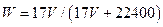
D.C=1000Vρ/(17V+22400)
参考答案:AB
本题解析:略
本题难度:一般
2、简答题 取A、B两份物质的量浓度相等的NaOH溶液,体积均为50 mL,分别向其中通入一定量的CO2后,再分别稀释为100 mL。
(1)在NaOH溶液中通入一定量的CO2后,溶液中溶质的组成可能是:
①________;②________;③________;④________。
(2)在稀释后的溶液中分别逐滴加0.1 mol/L的盐酸,产生的CO2的体积(标准状况)
与所加盐酸的体积关系如图所示:
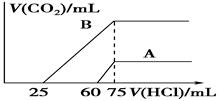
①分别加入足量的盐酸后的溶液中的溶质是________,原NaOH溶液的物质的量浓度为________。
②A曲线表明,原溶液通入CO2后,所得溶质与HCl反应产生CO2的最大体积是________mL(标准状况)。
③B曲线表明,原溶液通入CO2后,所得溶质的化学式为________,其物质的量之比为________。
参考答案:(1)①Na2CO3和NaOH;?②Na2CO3;③ Na2
本题解析:(1)氢氧化钠和CO2反应可逆生成正盐碳酸钠,或者酸式盐碳酸氢钠,所以溶液中溶质的组成可能是Na2CO3和NaOH;Na2CO3;Na2CO3和NaHCO3;NaHCO3。
(2)①如果加入足量的盐酸,则最终都生成氯化钠。根据图像可知,需要盐酸是75ml,所以氯化钠的物质的量是0.0075mol,所以根据原子守恒可知,氢氧化钠的物质的量是0.0075mol,因此原NaOH溶液的物质的量浓度为0.0075mol÷0.05L=0.15mol/L。
②由于碳酸钠和盐酸可以是分步进行的,所以根据曲线A
本题难度:一般
3、选择题 标准状况下,将11.2 L O2、11 g CO2、0.25 mol N2混合,则该混合气体的体积为(???)
A.2.24L
B.22.4 L
C.44.8 L
D.24.5 L
参考答案:B
本题解析: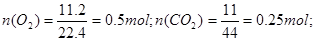 则混合气体中总物质的量为
则混合气体中总物质的量为
0.5mol+0.25mol+0.25mol=1mol,即正确答案为B,
本题难度:简单
4、选择题 下列溶液中溶质的物质的量浓度为1 mol・L-1的是(???? )
A.将40 g NaOH溶解于1 L水中配成的NaOH溶液
B.常温常压下将22.4 L HCl 气体溶于水配成1 L的盐酸溶液
C.将1 L 10 mol/L的浓盐酸与9L水混合配成溶液
D.从1000 mL 1 mol/L NaCl溶液中取出100 mL的溶液
参考答案:D
本题解析:A选项40gNaOH为1molNaOH但溶于一升水中不知最终溶液的体积c(物质的量浓度)=溶剂物质的量/溶液的体积故A不正确B选项是常温常压下只有在标准状况下22.4LHCL=1mol的HCL标况下盐酸溶液的物质的量浓度才为1mol/L ??? C选项仍不知混合后的溶液体积D选项取1mol/LNaCl的溶液任意毫升浓度不变故D正确
本题难度:简单
5、选择题 在10mL 0.05mol/L的某金属硫酸盐M2(SO4)x溶液中,滴加15mL 0.10mol/L的BaCl2溶液,恰好完全反应生成硫酸钡沉淀,该金属的化合价为
A.+1
B.+2
C.+3
D.不能确定
参考答案:C
本题解析:10mL× 0.05mol/L×x="15mL" ×0.10mol/L,解得x=+3,选C。
本题难度:一般