溶液呈血红色,含有铁元素
?
参考答案:B
本题解析:答案A加入盐酸,产生无色气体结论含铝、铁或铝、镁。加入NaOH 溶液只有铝反应产生无色气体,铁、镁不反应故正确。加入盐酸后,所得溶液中再加入少量NaOH溶液,也可能是沉淀A(OH)3, 加入KSCN 溶液,金属单质与之不反应,即便含铁元素溶液不会变色
本题难度:一般
2、实验题 (20分)某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计右图所示装置进行“铁与水反应”的实验。
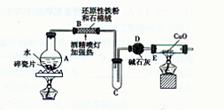 ????????????? ?????????????
(1)硬质试管中发生反应的化学方程式为????????。
(2)反应前A中投放碎瓷片的目的是????????。
(3)装置E中的现象是????????。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质试管B冷却后,取少许其中的固体物质溶于????????后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同)????????。;若溶液未变红色,推断硬质玻璃管B中固体物质的成分
①一定有Fe3O4,可能有Fe???②Fe3O4和Fe???③只有Fe3O4???④只有Fe
(6)另一份用___????????(填仪器名称)加入????????,可以证明溶液中存在Fe2+。
【探究三】设计如下流程利用上述滤液制取绿矾晶体(FeSO4・7H2O)。
滤液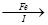 FeSO4溶液 FeSO4溶液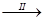 FeSO4・7H2O晶体 FeSO4・7H2O晶体
(7)步骤I中加入洁净废铁屑的作用是???????????????(用化学方程式表示)。
(8)步骤II从FeSO4稀溶液中得到FeSO4・7H2O晶体的主要操作包括????????、趁热过滤____、再过滤。为防止FeSO4变质,该流程中还需注意的问题有????????。
【探究四】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
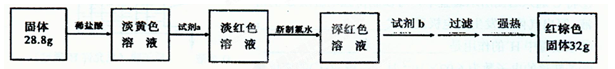
(9)试剂b的化学式是????????____。
(10)计算反应后B装置中铁元素的质量分数为????????;根据计算结果判断反应后硬质试管B中固体物质的成分是????????。
?????
参考答案:
 本题解析:略 本题解析:略
本题难度:简单
3、填空题
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
1.取混合物样品溶于水,分别取少量溶液进行以下实验
2._________________________________________则一定存在K+;
3.___________________________________________________则一定存在CO32―。
(二)测定K2CO3质量分数
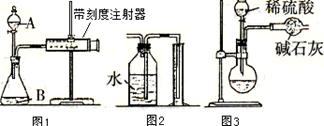
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是????????????????????????????????
????????????????????????????????????????????????????????????????????????。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数???????(填“偏大”、“偏小”、“不变”),你的改进方案是???????????????????????????????????????。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I??????????????????????????????????????????????????;
Ⅱ???????????????????????????????????????????????????????????????????????
Ⅲ???????????????????????????????????????????????????????????????????????
参考答案:(一)2. 用焰色反应,同时透过钴玻璃片观看燃烧的火焰,如果
本题解析:略
本题难度:简单
4、判断题 如下图中①―11分别代表有关反应物中的一种物质,请填写以下空白。
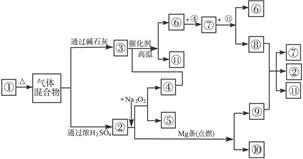
(1)①③④的化学式分别是___________、___________、___________。
(2)⑧与⑨反应的化学方程式是________________________________________________。
(3)②与Mg条(点燃)反应的化学方程式为:__________________________________。
参考答案:(1)NH4HCO3? NH3? O2
(2)C+4H
本题解析:由②+Mg ⑨+⑩,想到中学化学的典型反应CO2+2Mg====C+2MgO知②为CO2(突破口) ⑨+⑩,想到中学化学的典型反应CO2+2Mg====C+2MgO知②为CO2(突破口)
由:②+Na2O2 ④+⑤,且②为CO2知④、⑤为Na2CO3和 O2 ④+⑤,且②为CO2知④、⑤为Na2CO3和 O2
由:③+④ ⑥+?B11?,知④为O2则⑤为Na2CO3,③为NH3。 ⑥+?B11?,知④为O2则⑤为Na2CO3,③为NH3。
其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,
⑧为HNO3,⑨为C,⑩为MgO,?B11?为H2O。
本题难度:简单
5、选择题 下列实验数据记录和实验方法正确的是(????)????????????????? A.用天平称取4.0gNaOH固体,用100mL量筒配制1.00mol/L的NaOH溶液
B.用25mL的滴定管(内装有标准NaOH溶液)滴定未知浓度的盐酸用去NaOH溶液22.32mL
C.用pH试纸测得新制氯水的pH为4
D.常温下,用气球收集500mLNO2气体,求得NO2气体的物质的量为(0.5/22.4)mol
参考答案:B
本题解析:
本题难度:简单
|
|