��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��8�֣��������ʵ�����A��B�����1 L���ܱ������У��������·�Ӧ
3A(g)��B(g)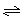 ?xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)����
?xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)����
(1)��ʱA��Ũ��c(A)��________mol/L����Ӧ��ʼǰ�����е�A��B�����ʵ�����n(A)��n(B)��________mol��
(2)B��ƽ����Ӧ����v(B)��________mol/(L��min)��?
(3)x��ֵΪ________��
�ο��𰸣�(1)0.75��1.5???? (2)0.05??????
���������������淴Ӧ���йؼ��㡣
��1��C��ƽ����Ӧ������0.1mol/(L��min)����C��Ũ����0.5mol/L�����Ը��ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪x��2������Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����B�ķ�Ӧ������0.1mol/(L��min)��2��0.05mol/(L��min)��
��2��??????????? 3A��g��+B(g) 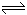 2C(g)+2D(g)
2C(g)+2D(g)
��ʼ����mol��??? n??????? n?????? 0????? 0
ת������mol��?? 0.5????? 0.25????? 0.5??? 0.5
ƽ������mol��? n��0.75?? n��0.25?? 0.5??? 0.5
������n��0.75���U��n��0.25���� 3:5
���n��1.5mol������A��Ũ����0.75mol��1L��0.75mol/L
�����Ѷȣ�һ��
2��ʵ���� ��11�֣�ij�о���ѧϰС��Ϊ֤��2Fe3+ + 2I-  ?2Fe2+ + I2Ϊ���淴Ӧ������Ӧ����һ�����ȣ���������¼��ַ�������֪FeF63-��һ����ɫ���ȶ��������ӡ�
?2Fe2+ + I2Ϊ���淴Ӧ������Ӧ����һ�����ȣ���������¼��ַ�������֪FeF63-��һ����ɫ���ȶ��������ӡ�
��Ҫ��ش��������⡣
�����ף�
ȡ5mL 0.1mol/L KI��Һ���μ�2ml 0.1mol/L ��FeCl3��Һ���ټ�������2mL CCl4����������á��ֲ㣬��ȡ�ϲ���Һ���μ�KSCN��Һ��
��1����������֤���÷�ӦΪ���淴Ӧ��������????????????????????????????��
��2����ͬѧ��Ϊ�÷�����Ʋ������ܣ���ʹ�÷�ӦΪ�����淴ӦҲ���ܳ�������������ԭ����????????????????????????????????��
�����ң�
ȡ5mL 0.1mol/L KI��Һ���μ�2ml 0.1mol/L ��FeCl3��Һ����Һ���ػ�ɫ��������Һ�еμ�NH4F��Һ��������???????????????????������֤���÷�ӦΪ���淴Ӧ������Ͳ����������ԭ��???????????????????????????????????????��
��������
�����ͼԭ���װ�ã���ͨ���������ƣ�ָ������ƫת��ע������������ָ������ƫ���Դ������������ʱ����е����ƶ�����С����������Ϊ�㡣
��ָ���������������ձ��м���1mol/L FeCl2��Һ�����۲쵽���������Ƶ�ָ����?????����ƫת��������ҡ����ƶ������������жϸ÷�ӦΪ���淴Ӧ����ʱ����ʯī�缫�ϵĵ缫��ӦʽΪ???????????????????????????��
�ο��𰸣���1���²㣨CCl4�㣩��Һ���Ϻ�ɫ�����ϲ���Һ�еμ�KSC
�����������1������ʵ�����ݿ�֪�⻯���ǹ����ģ�����Ӧ�ǿ��淴Ӧ������Һ��һ�����������ӣ�ͬʱҲ�������ɵ��ʵ⡣���Կ���ͨ�����������Ӻ͵��ʵ���֤����
��2����Ϊ�����Ӻ����������ڿ�����Ҳ���Ա������������ɵ��ʵ�������ӣ����Է������Ǻ����ܡ�
��3�������������������ƽ���Ӱ������֤����ΪFe3+��F-���������ɫ��FeF63-����ʹ2Fe3+ + 2I-  ?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ���������Һ��ɫ���dz��
?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ���������Һ��ɫ���dz��
��4����ԭ����и�����ʧȥ���ӵģ�������ʧȥ���ӣ����Ե����ǴӼ׳������ҳأ����Ե����Ƶ�ָ������ƫת��
�����Ѷȣ�һ��
3��ѡ���� һ�������£����淴Ӧ2A B��3C������������״̬�У�����ƽ��״̬����(����)��
B��3C������������״̬�У�����ƽ��״̬����(����)��
?
| ����Ӧ����
| �淴Ӧ����
|
A
| vA��2 mol��L��1��min��1
| vB��2 mol��L��1��min��1
|
B
| vA��2 mol��L��1��min��1
| vC��2 mol��L��1��min��1
|
C
| vA��1 mol��L��1��min��1
| vB��2 mol��L��1��min��1
|
D
| vA��1 mol��L��1��min��1
| vC��1.5 mol��L��1��min��1
?
�ο��𰸣�D
������������淴Ӧ���ʸ��ݻ�ѧ����ʽͳһ�����A��ʾ�ķ�Ӧ���ʣ���A���������ʡ�D�����Ӧ���ʼ�A����������vA��1 mol��L��1��min��1���淴Ӧ����vC��1.5 vA(��)��vA(��)��1 mol��L��1��min��1������ȣ�˵����Ӧ�ﵽ��ƽ��״̬��
�����Ѷȣ���
4��ѡ���� ��1molSO2��1molO2ͨ��һ���������ܱ������У���һ���¶Ⱥʹ��������£���Ӧ�ﵽƽ�⣬SO3Ϊ0��3mol����ʱ������0��5molO2��0��5molSO2����Ӧ�ﵽ�µ�ƽ��ʱ��SO3�����ʵ���Ϊ [???? ]
A��0��3 mol
B��0��15 mol
C��С0��15mol
D������0��15mol����0��3mol
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� �����£��ݻ���Ϊ2L���ܱ�����M��N�У��ֱ�������������ʼͶ�Ͻ����Ŀ��淴Ӧ
3A(g)+2B(g)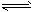 2C(g)+xD(s)�Ļ�ѧƽ��״̬������������£�M�г�ʼ����3mol A��2mol B��2min��ﵽƽ��ʱ����1. 2mol D����ôӷ�Ӧ��ʼ��ƽ�⣬C������Ϊ 0. 3mol/(L��min)��N�г�ʼ����2molC�� 2C(g)+xD(s)�Ļ�ѧƽ��״̬������������£�M�г�ʼ����3mol A��2mol B��2min��ﵽƽ��ʱ����1. 2mol D����ôӷ�Ӧ��ʼ��ƽ�⣬C������Ϊ 0. 3mol/(L��min)��N�г�ʼ����2molC��
ymolD���ﵽƽ��ʱc(A) =0. 6mol/L�������ƶ���ȷ���� [???? ]
A��x=2
B��ƽ��ʱ��M��c(A)<0.6mol/L
C��y>0.8?
D��v<0.8
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
|