微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知热化学反应方程式:2H2(g)+O2(g)===2H2O(g) ΔH1=-483.6 kJ/mol则对于热化学方程式:
2H2O(l)===2H2(g)+O2(g) ΔH2 下列说法正确的是
[???? ]
A.热化学方程式中化学计量数表示分子个数
B.该反应的ΔH2=+483.6 kJ/mol
C.|ΔH2|<|ΔH1|
D.|ΔH2|>|ΔH1|
参考答案:D
本题解析:
本题难度:简单
2、填空题 (10分) I.已知下列三个热化学方程式
①H2(g)+O2(g)===H2O(g) ΔH=-241.8 kJ・mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ・mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131 kJ・mol-1
写出表示碳不完全燃烧生成CO的热化学方程式。__________;
II. 氨气溶于水得到氨水,在25℃下,将a mol・L-1的氨水与b mol・L-1的盐酸等体积混合,反应后溶液显中性,则用含a和b的代数式表示出该混合溶液中氨水的电离平衡常数 。
III.下列5种有机化合物:水杨酸( )、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应的是 。(填化学式)
②其中能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应的是 。(填化学式)
③写出水杨酸与金属钠反应的化学方程式 。
参考答案:C(s)+O2(g)===CO(g) ΔH
本题解析:I.根据盖斯定律可知,①+③即得到C(s)+O2(g)==="CO(g)" ,所以反应热是△H=-241.8 kJ・mol-1+131 kJ・mol-1=-110.8 kJ・mol-1。
II.反应后显中性,说明氨水过量。剩余氨水的浓度是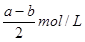 ,根据电荷守恒可知,溶液中NH4+浓度是
,根据电荷守恒可知,溶液中NH4+浓度是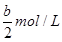 、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K=
、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K=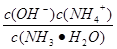 =
=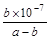 。
。
III.考查常见官能团的性质。
①能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应,说明含有羧基,但不能含有酚羟基,所以应该是乙酸。
②能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应,说明含有酚羟基,但没有羧基,所以应该是苯酚。
本题难度:困难
3、填空题 根据下列反应的焓变,计算C(石墨)与H2(g)反应生成1molC2H2(g)的焓变(△H)。
C(石墨)+ O2(g)=CO2(g) △H1="a" kJ・mol-1
2H2(g)+O2(g)=2H2O(l) △H2="b" kJ・mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3="c" kJ・mol-1
△H= 。
参考答案:△H=2a+b/2-c/2 kJ・mol-1
本题解析:
试题分析:根据盖斯定律可知,①×2+②÷2-③÷2即得到反应2C(石墨)+H2(g=C2H2(g),则该反应的△H=2a+b/2-c/2 kJ・mol-1。
考点:考查反应热的计算
点评:该题是基础性试题的考查,也是高考中的常见题型和考点。该题的关键是利用好盖斯定律,有利于培养学生的逻辑推理能力和规范的答题能力。
本题难度:一般
4、填空题 (6分)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下:

根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为 。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) ΔH = -90.8kJ・mol-1
CH3OH(g) ΔH = -90.8kJ・mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH = -23.5kJ・mol-1
CH3OCH3(g)+H2O(g) ΔH = -23.5kJ・mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH = -41.3kJ・mol-1
CO2(g)+H2(g) ΔH = -41.3kJ・mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH = 。
CH3OCH3(g)+CO2(g);ΔH = 。
(3)某科研机构研制的一种新型的质子交换膜二甲醚燃料电池(DDFC),该电池有较高的安全性。该电池总反应为CH3OCH3+3O2=2CO2+3H2O,其工作原理如图所示。
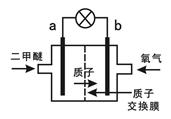
电极a的电极反应式为 。
参考答案:(1)CH4+H2O 本题解析:
本题解析:
试题分析:(1)从流程图看出CH4和H2O在催化剂的作用下反应生成了 CO和H2,化学方程式为:CH4+H2O CO+3H2 (2)①×2+②+③可得总反应,则ΔH =-90.8×2-23.5-41.3=-246.4kJ・mol-1[来(3)在燃料电池中,燃料反应的一极是负极,氧气反应的一极是正极,所以a是负极,失去电子,电极反应为:CH3OCH3-12e-+3H2O
CO+3H2 (2)①×2+②+③可得总反应,则ΔH =-90.8×2-23.5-41.3=-246.4kJ・mol-1[来(3)在燃料电池中,燃料反应的一极是负极,氧气反应的一极是正极,所以a是负极,失去电子,电极反应为:CH3OCH3-12e-+3H2O 2CO2+12H+[
2CO2+12H+[
考点:根据条件书写化学方程式、热化学方程式的计算、燃料电池电极反应的书写。
本题难度:困难
5、填空题 为实现 “节能减排” 和“低碳经济”的一项课题是如何将CO2转化为可利用资源。
(1)25℃,1.01×105Pa时,16g液态甲醇(CH3OH)完全燃烧,当恢复到原状态时,放出热量363.3kJ,该反应的热化学方程式为 。
(2)目前,工业上常用CO2来生产燃料甲醇。现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。
测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①该反应的平衡常数表达式K= ;
②从反应开始到平衡时,CH3OH的平均反应速率v(CH3OH)= (注明单位);H2的转化率= ;
③下列说法中,能说明上述反应达到平衡状态的是
A.每消耗1mol CO2的同时生成1mol CH3OH
B.CO2、H2、CH3OH和H2O的物质的量的比为1∶3∶1∶1
C.容器中气体的压强不再改变
D.容器中气体的密度不再改变
④下列措施中,能使上述平衡状态向正反应方向移动的是
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用高效催化剂 D.恒温恒容再充入1 molCO2和3 mol H2
参考答案:(1)CH3OH(l)+ 本题解析:
本题解析:
试题分析:(1)由m/M可知,n(CH3OH)=1/2mol,则1/2 CH3OH (l)+3/4O2(g)==1/2CO2(g)+H2O(l) △H=―363.3kJ/mol,系数加倍可得,CH3OH(l)+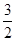 O 2(g)=CO2(g)+2H2O(l) △H=-726.6kJ/mol;(2)①K=
O 2(g)=CO2(g)+2H2O(l) △H=-726.6kJ/mol;(2)①K=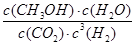 ;②读图可知,v(CH3OH)=
;②读图可知,v(CH3OH)=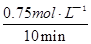 =0.075mol?L―1?min―1;由于v(H2)="3" v(CH3OH)= 0.225mol?L―1?min―1,则△n(H2)= 0.225mol?L―1?min―1×10min×1L=2.25mol,H2的转化率=2.25/3×100%=75%;③均为正反应速率,故A错;不能说明各组分的物质的量保持不变,故B错;能说明各组分的物质的量保持不变,故C正确;由于各组分都是气体且恒容,则混合气体的密度始终不变,故D错;④正反应放热,升高温度平衡左移,故A错;减小生成物浓度,平衡右移,故B正确;催化剂不能使平衡移动,故C错;相当于增大压强,正反应气体体积减小,则平衡右移,故D正确。
=0.075mol?L―1?min―1;由于v(H2)="3" v(CH3OH)= 0.225mol?L―1?min―1,则△n(H2)= 0.225mol?L―1?min―1×10min×1L=2.25mol,H2的转化率=2.25/3×100%=75%;③均为正反应速率,故A错;不能说明各组分的物质的量保持不变,故B错;能说明各组分的物质的量保持不变,故C正确;由于各组分都是气体且恒容,则混合气体的密度始终不变,故D错;④正反应放热,升高温度平衡左移,故A错;减小生成物浓度,平衡右移,故B正确;催化剂不能使平衡移动,故C错;相当于增大压强,正反应气体体积减小,则平衡右移,故D正确。
考点:本题考查热化学方程式、化学反应速率和化学平衡。
本题难度:困难