微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在氯化铵溶液中,下列关系正确的是(??)。
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
C.C(Cl-)=C(NH4+)>C(H+)=C(OH-)
D.C(NH4+)=C(Cl-)>C(H+)>C(OH-)
2、填空题 (14分)常温下钛的化学活性很小,在较高温度下可与多种物质反应。工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:
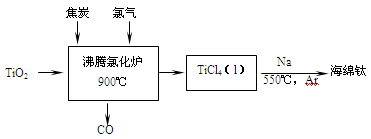
(1)TiCl4遇水强烈水解,写出其水解的化学方程式 。
(2)①若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
②Cl2含量检测仪工作原理如下图,则Cl2在Pt电极放电的电极反应式为 。

③实验室也可用KClO3和浓盐酸制取Cl2,方程式为:KClO3 + 6HCl(浓) =" KCl" + 3Cl2↑+ 3H2O。
当生成6.72LCl2(标准状况下)时,转移的电子的物质的量为 mol。
(3)一定条件下CO可以发生如下反应:4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。
①该反应的平衡常数表达式为K= 。
②将合成气以n(H2)/n(CO)=2通入1 L的反应器中,CO的平衡转化率随温度、压强变化关系如图所示,下列判断正确的是 (填序号)。
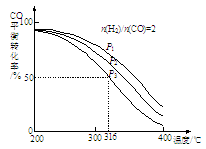
a.△H <0
b.P1<P2<P3
c.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
③采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(简称DME)。观察下图回答问题。
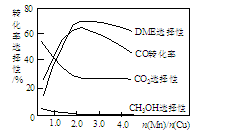
催化剂中n(Mn)/n(Cu)约为 时最有利于二甲醚的合成。
3、选择题 下列关于电解质溶液的叙述不正确的是
A.常温下,pH=7的CH3COONa与CH3COOH的混合溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)= c(OH-)
B.将pH=10的氨水稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量前者小于后者
D.常温下,同浓度的Na2CO3溶液与NaHCO3溶液相比,Na2CO3溶液的pH较大
4、填空题 (6分)下列盐溶液能发生水解的用离子方程式表示,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性
K 2CO3 , 溶液呈 性;
Na2SO4 , 溶液呈 性;
CuCl2 , 溶液呈 性。
5、选择题 T℃时,某浓度醋酸钠溶液的pH=10,下列说法一定正确的是
A.溶液中由水电离出的OH一离子浓度c(OH一)=1×10一10mol/L
B.溶液中存在:c(H+)・c(OH一)=l×10-14(mol/L)2
C.溶液中存在:c(Na+)>c(CH3COO一)>c(OH一)>c(H+)>c(CH3COOH)
D.溶液中存在:c(CH3COOH)+c(CH3COO一)=c(Na+)