微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
A.6.72 L
B.11.2 L
C.22.4 L
D.4.48 L
参考答案:A
本题解析:
试题分析:合金溶于足量的NaOH溶液中,金属铝和氢氧化钠反应产生气体氢气3.36L(标准状况)物质的量为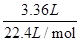 =0.15mol,根据电子转移守恒可知n(Al)=
=0.15mol,根据电子转移守恒可知n(Al)= 本题难度:一般
本题难度:一般
2、填空题 在 K2Cr2O7 + 14HCl ="===" 2KCl + 2CrCl3 + 3Cl2?+ 7H2O反应中。
="===" 2KCl + 2CrCl3 + 3Cl2?+ 7H2O反应中。
(1)????元素被氧化,????是氧化剂,氧化产物是?????????;
(2)此反应若转移了12mol的电子,则生成氯气???????L(标准状况)
参考答案:(1)Cl, K2Cr2O7, Cl2?;(2) 134.4
本题解析:略
本题难度:简单
3、选择题 某工厂利用FeCl3溶液腐蚀镀有铜的绝缘板生产电路板,一实验小组对该厂生产电路后所得的废液进行分析。取50.0 mL废液,向其中加入0.64 g Cu,金属铜全部溶解。另取50.0 mL废液,向其中加入足量的AgNO3,析出沉淀43.05 g,下列说法正确的是(??)
A.原废液中含有的金属阳离子只有Fe2+和Cu2+
B.该工厂原来使用的FeCl3溶液的物质的量浓度约为2 mol/L
C.若向500 mL废液中加入足量的稀HNO3溶液,在标况下产生NO气体4.48 L,则原废液中Fe2+和Cu2+的物质的量浓度之比为2:1
D.可以使用硫氰化钾溶液检验该废液中是否含有Fe2+
参考答案:BC
本题解析:
试题分析:有题干信息可知,铜是0.01mol全部溶解,应该有0.02molFe3+,A错误;对第二份溶液分析,可知氯离子=氯化银=43.05/(108+35.5)= 0.3mol ,该工厂原来使用的FeCl3溶液的物质的量浓度约为C=0.1 mol /0.05 L ="2" mol/L.B正确;对于500ml产生了0.2molNO,那么在50ml中应该可以得到0.06mol电子.这0.06mol应该是Fe2+ ,溶液中有至少0.02molFe3+, 0.06molFe2+ ,0.3mol Cl-.
本题难度:一般
4、选择题 在某100 mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.4 mol/L、
0.1 mol/L,向该混合液中加入1.92 g铜粉,加热,待充分反应后,所得溶液中铜离子物质的量浓度是(??)
A.0.15 mol/L
B.0.225 mol/L
C.0.30 mol/L
D.0.45 mol/L
参考答案:B
本题解析:溶液中同时存在H+和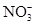 时就能够与Cu发生反应。该溶液中 H+实际为 0.06 mol,应该根据离子方程式进行计算,正确解题思路为:
时就能够与Cu发生反应。该溶液中 H+实际为 0.06 mol,应该根据离子方程式进行计算,正确解题思路为:
3Cu?? +?? 8H+?????+??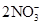
本题难度:一般
5、选择题 水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+a OH-=Y+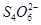 +2H2O下列说法中,不正确的是??(???)
+2H2O下列说法中,不正确的是??(???)
A.S2O32-是还原剂
B.Y的化学式为Fe2O3
C.a=4
D.每有1mol O2参加反应,转移的电于总数为4 mol
参考答案:B
本题解析:
试题分析:根据题意可知:Fe2+和S2O32-作还原剂失去电子。氧气得到电子作氧化剂。每有1mol O2参加反应,转移的电于总数为4 mol结合原子守恒可得Y的化学式为Fe3O4,a=4.选项为 :B。
本题难度:一般