��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� NOx������β���е���Ҫ��Ⱦ��֮һ��
��1�� NOx���γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ:_ .
��2����������������ʱ������N2��02��Ӧ���������仯ʾ��ͼ����:
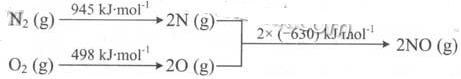
��д���÷�Ӧ���Ȼ�ѧ����ʽ: _ .
�����¶����ߣ��÷�Ӧ��ѧƽ�ⳣ���ı仯������_ .��
��3��������β��ϵͳ��װ�ô�ת����������Ч����NOX���ŷš�
�ٵ�β���п�������ʱ��NOX�ڴ�ת�����б���ԭ��N2�ų���д��NO��CO��ԭ�Ļ�ѧ����ʽ��_ .
�� ��β���п�������ʱ����ת�����еĽ�������������NOX�����Ρ�����������˳�����£�12MgO <2oCaO <38SrO<56BaO.ԭ���� .
��4��ͨ��NOx�������ɼ��NOx�ĺ������乤��ԭ��ʾ��ͼ����:

��Pt�缫�Ϸ������� ��Ӧ(���������ԭ��)��
��д��NiO�缫�ĵ缫��Ӧʽ: .
�ο��𰸣�
��1��3NO2+H2O=2HNO3+NO
��2
�����������NO2�Ʊ�����3NO2+H2O===2HNO3+NO���������������ϵ�ɵõ��Ȼ�ѧ��Ӧ����ʽN2(g)+O2(g) 2NO(g) ��H="+183kJ/mol" ,�÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���Kֵ����һ��������һ����̼�ķ�Ӧ���ɵ���2NO+2CO= N2+2CO��Mg��Ca��Sr��BaΪͬһ����Ԫ�أ����ϵ��£�ԭ�Ӱ뾶������Ԫ�صĽ���������ǿ�������������NOX��������������ǿ���绯ѧ��ӦPt�缫Ϊ����������ԭ��Ӧ��O2+4e-=2O2-,NiO�缫Ϊ��������������ӦNO-2e-+O2-=NO2��
2NO(g) ��H="+183kJ/mol" ,�÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���Kֵ����һ��������һ����̼�ķ�Ӧ���ɵ���2NO+2CO= N2+2CO��Mg��Ca��Sr��BaΪͬһ����Ԫ�أ����ϵ��£�ԭ�Ӱ뾶������Ԫ�صĽ���������ǿ�������������NOX��������������ǿ���绯ѧ��ӦPt�缫Ϊ����������ԭ��Ӧ��O2+4e-=2O2-,NiO�缫Ϊ��������������ӦNO-2e-+O2-=NO2��
��1��NOx���γ����꣬NO2ת��ΪHNO3�Ļ�ѧ����ʽΪ3NO2+H2O=2HNO3+NO.
��2���ٸ�˹���ɿɵã��÷�Ӧ���Ȼ�ѧ����ʽΪN2(g)+O2(g) 2NO(g)����H=+183kJ/mol.
2NO(g)����H=+183kJ/mol.
�ڸ÷�ӦΪ���ȷ�Ӧ�����¶����ߣ��÷�Ӧ��ѧƽ�ⳣ��Kֵ����
��3��������β��ϵͳ��װ�ô�ת����������Ч����NOX���ŷš�
��NO��CO��ԭ�Ļ�ѧ����ʽΪ2NO+2CO= N2+2CO.
��Mg��Ca��Sr��BaΪͬһ����Ԫ�أ����ϵ��£�ԭ�Ӱ뾶������Ԫ�صĽ���������ǿ�������������NOX��������������ǿ��Ԫ�صĽ���������ǿ�������������NOX��������������ǿ��
��4����Pt�缫�Ϸ������ǻ�ԭ��Ӧ����NiO�缫�ĵ缫��ӦʽΪNO-2e-+O2-=NO2��
�����㶨λ�������Ե���������Ϊ���忼���������ʡ��Ȼ�ѧ��Ӧ����ʽ��Ԫ���������Լ�Ԫ�����ڱ����绯ѧ�����֪ʶ��
�����Ѷȣ�����
2��ѡ���� ���ܱ������е�һ����������巢����Ӧ��xA��g��+yB��g�� zC��g��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.30 mol/L�������й��жϲ���ȷ���� �� ��
zC��g��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.30 mol/L�������й��жϲ���ȷ���� �� ��
A��x+y
�ο��𰸣�
���������
�����Ѷȣ�һ��
3������� ˮ������֮Դ��Ҳ�ǻ�ѧ��Ӧ�е����ǣ���ش��������⣺
������ȼ������Һ̬ˮ�Ȼ�ѧ����ʽ��2H2��g��+O2��g���T2H2O��l����H=-572kJ/mol��
��1�������������ܺ�______������ڡ�����С�ڡ����ڡ�����Ӧ�������ܺͣ�
��2����2mol������ȫȼ������ˮ��������ų�������______572kJ�����������������=������
��3��������ֵΪ______��
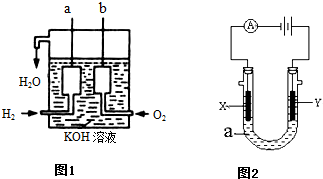
��������������Ӧ����ˮ������ѧ��ת��Ϊ���ܣ��乹����ͼ1��ʾ��a��b�����缫���ɶ��̼����ɣ�
��1��a�缫��Ӧʽ��______
��2��b�缫��Ӧʽ��______
��ͼ2��ʾһ�����أ�X��Y���Ƕ��Ե缫�����Һa�DZ���ʳ��ˮ��ͬʱ�����߸����뼸�η�̪��Һ��
��1��X���ϵĵ缫��ӦʽΪ______����X�������۲쵽��������______��
��2��Y���ϵĵ缫��ӦʽΪ______������õ缫��Ӧ����ķ�����______��
�ο��𰸣���1���÷�Ӧ����ӦΪ���ȷ�Ӧ���������������С�ڷ�Ӧ������
���������
�����Ѷȣ�һ��
4������� �������ⱸ�������ע���������Լ�����β���ŷŵ�һ����̼��CO�����������NOx������������强��Ϊ������Ⱦ����Ҫ���أ�
��1��CO���ж�������CO��ѪҺ��Ѫ�쵰��Ѫ���ز��ַ�Ӧ����̼��Ѫ�쵰�ף���Ӧ����ʽ�ɱ�ʾΪ��CO+Hb?O2??

?O2+Hb?CO
ʵ�������c��Hb?CO����ʹֻ��c��Hb?O2����?1/50��Ҳ������˵��������ˣ�
��֪t��ʱ������Ӧ��ƽ�ⳣ��K=200������β�O2��Ũ��ԼΪ1.0��10-2mol?L-1����ʹc��Hb?CO��С��c��Hb?O2����?1/50��������β�CO��Ũ�Ȳ��ܳ���______mol?L-1��
��2������β�������ķ���֮һ�����������������ϰ�װһ������ת��������
��֪��Ӧ2NO��g��+2CO��g��?

??N2��g��+2CO2��g����H=-113kJ?mol-1
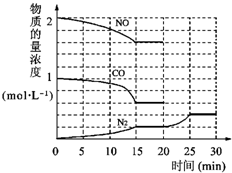
��Ϊ��ģ���ת�����Ĺ���ԭ������t��ʱ����2molNO��1mol?CO����lL��Ӧ�����У���Ӧ������NO��g����CO��g����N2��g�����ʵ���Ũ�ȱ仯������ͼ��ʾ����Ӧ���е�15minʱ��NO��ƽ����Ӧ����Ϊ______��
�ڹ۲���20min��30min��N2��g�������仯������ͼ���ж�����ñ仯������������______��
a���������
b��������ϵ�¶�
c����С�������Ϊ0.5L
d������CO2�����ʵ���
��3��ú�����г����о���ͬ�¶���ƽ�ⳣ����Ͷ�ϱȼ����ʵ����⣮
��֪��CO��g��+H2O��g��?

H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 830 | 1000
ƽ�ⳣ��K
10
9
1
0.6
�Իش���������
����������Ӧ�ǣ�______��Ӧ������ȡ��������ȡ�����
��ij�¶���������Ӧƽ��ʱ�����ݡ������¶ȣ�����Ӧ����______�����������С�����䡱���������ڻ�������ѹǿ______�����������С�����䡱����
����830�淢��������Ӧ�����±��е����ʵ���Ͷ����ݷ�Ӧ��������������Ӧ�����ƶ�����______��ѡ��A��B��C��D����
| A | B | C | D
n��CO2��
3
1
0
1
n��H2��
2
1
0
1
n��CO��
1
2
3
0.5
n��H2O��
5
2
3
2
�ο��𰸣���1������ƽ�ⳣ�����㣬K=
���������
�����Ѷȣ�һ��
5��ѡ���� X��Y��Z��������̬���ʣ���һ���¶�����仯������ͼ������˵��һ����ȷ����
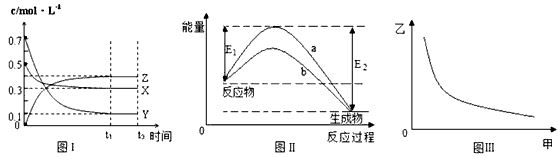 [???? ] [???? ]
A���÷�Ӧ�Ȼ�ѧ����ʽΪX(g) +3Y(g) 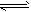 ?2Z(g) ��H= -��E2-E1�� ?2Z(g) ��H= -��E2-E1��
B����ͼIII�мױ�ʾѹǿ���ұ�ʾZ�ĺ���������仯����ͼIII������
C���������¶ȣ��÷�Ӧ��ƽ�ⳣ����С��Y��ת���ʽ���
D��ͼII������b�Ǽ������ʱ�������仯���ߣ�����aһ����û�м������ʱ�������仯����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
|
|