微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
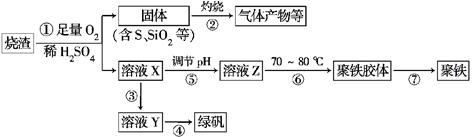
1、填空题 化工生产中常利用硫酸厂煅烧黄铁矿石的烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)来制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4・7H2O),流程如?????下:
 ?
?
(1)将过程②中产生的气体通入下列溶液中,溶液会褪色的是________(填选项序号)。
a.品红溶液? b.紫色石蕊溶液?? c.酸性KMnO4溶液? d.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为______________________
(3)过程③中,需加入的物质是____________;反应的化学方程式为_____________________
用溶液Y制绿矾时,可取少量Y溶液于试管中,向试管内加入少量的________________溶液,观察溶液是否变为________色,以验证其中是否含有Fe3+。
(4)在实验室里,完成过程④中的____________(填操作名称),需要使用酒精灯、三脚架、坩埚钳等,还需要的玻璃仪器有___________________________。
(5)过程⑥中,将溶液Z加热到70~80℃,目的是____________________________________________________。
(6)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验:①用分析天平称取2.700 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495 g。若该聚铁的主要成分为[Fe(OH)SO4]n,则聚铁样品中铁元素的质量分数为________。(假设杂质中不含铁元素和硫元素)
参考答案:(1)acd (2)4FeS+3O2+12H+=4Fe3++
本题解析:由题中信息可知,过程①向烧渣中加稀硫酸并同时通入氧气,铁的氧化物、硫化亚铁均会溶解,生成硫酸铁、单质硫和水,所以溶液X是硫酸铁溶液,过程②灼烧固体,其中的硫被氧化成二氧化硫。(1)二氧化硫能分别使品红溶液、酸性KMnO4溶液和溴水褪色。(2)过程①中,FeS和O2、H2SO4反应的离子方程式为4FeS+3O2+12H+=4Fe3++6H2O+4S。(3)由产物绿矾逆推可知过程③是将硫酸铁转化为硫酸亚铁的过程,应加入铁粉还原硫酸铁,有关反应的化学方程式为Fe2(SO4)3+Fe=3FeSO4。验证硫酸亚铁溶
本题难度:困难
2、选择题 用类推的方法可能会得出错误结论,因此推出的结论要经过实践的检验才能确定其正确与否.下列类推结论中正确的是[???? ]
A.Na失火不能用CO2灭火,K失火不能用CO2灭火
B.工业上电解熔融MgCl2制取金属镁,也用电解熔融AlCl3的方法制取金属铝
C.Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3
D.Fe3O4可以写成FeO・Fe2O3,Pb3O4也可写成PbO・Pb2O3
参考答案:A
本题解析:
本题难度:简单
3、填空题 铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用。
(1)用铁屑与稀硫酸反应制备FeSO4
①制备原理用离子方程式表示为????????。若要提高FeSO4生成速率,采取下列措施中正确的是????????。
A.使用浓硫酸与铁屑反应???
B.使用磨细的铁粉反应
C.控制温度在50~70℃?????
D.控制温度在80~100℃
②在上述反应过程中,常会伴随发生反应:4Fe2++O2+4H+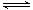 4Fe3++2H2O?
4Fe3++2H2O?
若要减少产品FeSO4中Fe3+的含量,采取下列措施中正确的是????????。
A.控制稀硫酸的浓度不能太高?????
B.用去O2蒸馏水注入浓硫酸配制反应所需的稀硫酸
C.反应中保持n(Fe)/n(H2SO4) >1???
D.反应中应经常添加Fe2(SO4)3搅拌
③反应结束后,将溶液进行??????????、冷却、过滤、洗涤即得FeSO4・7H2O晶体。
(2)工业上用含有少量Cu、Al的废铁屑制备Fe2(SO4)3
其反应及操作流程如下:
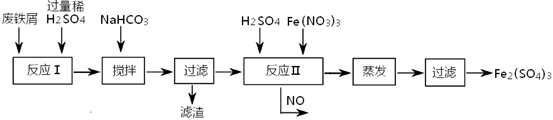
①加入NaHCO3并搅拌,将混合液pH调控至???????范围内,使杂质沉淀过滤除去。
沉淀物
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
| Cu(OH)2
|
开始沉淀
| 2.3
| 7.5
| 3.4
| 4.7
|
完全沉淀
| 3.2
| 9.7
| 4.4
| 6.7
?
②反应Ⅱ中反应的离子方程式是:???????????。
③生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是???????,气体X与NO配比的比例是???????。
(3)用Fe2(SO4)3处理含S2-污水时,有黑色沉淀及淡黄色悬浮物产生,其反应的离子方程式是?????????。
参考答案:(1)①? Fe+2H+=Fe2++H2↑???? B、C?
本题解析:
试题分析:(1)铁和氢离子发生置换反应制备硫酸亚铁,可以使用铁粉增大接触面积,加快速率,B正确;但是不能用浓硫酸,铁在常温条件下遇浓硫酸钝化,A错误;硫酸亚铁在60℃时溶解度高,所以选择温度在50~70℃,C正确,D错误。减少Fe2+被氧化,控制硫酸浓度,减少H+浓度,平衡逆向移动,A正确,B、稀释浓硫酸应该把硫酸向水中加,并不断搅拌,错误;C、铁过量可以防止Fe2+被氧化,正确;D、加入Fe3+将会增加Fe3+浓度,错误。反应结束后,过滤除去过量的铁,再降低温度,硫酸亚铁的溶解度减小,析出晶体。
本题难度:困难
4、填空题 从辉铜矿(Cu2S)中利用火法炼铜可以提取铜,发生如下反应:

下面是由Cu2S冶炼铜及制取CuSO4・5H2O的流程图:
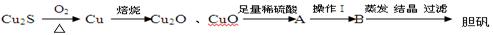
⑴Cu2S中铜元素的化合价为??,当有1molCu2S与O2反应生成2molCu时,转移电子的物质的量是?????????。
⑵Cu2O、CuO中加入足量稀硫酸得到的体系A中看到溶液呈蓝色,且有红色物质生成,请写出生成红色物质的离子方程式??????????????????????????????????????????????。
⑶若使A中单质溶解,操作Ⅰ中加入的试剂最好是???????。(选填字母代号)
A.适量的HNO3???? B.适量的NaOH???? C.适量的H2O2
该反应的离子方程式为?????????????????????????????????。
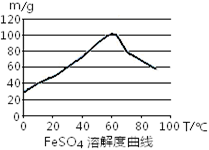
⑷取5.00?g胆矾样品逐渐升高温度使其分解,分解过程的热重曲线(样品质量随温度变化的曲线)如下图所示:

①由图中可以看出,胆矾分解的最低温度是???????。
②通过计算确定258℃时发生反应的化学方程式为??????????????????????????????????,e点对应的化学式为?????????(计算过程略去)。
参考答案:(1)+1 、 6mol??(2)Cu2O + 2H+ ="
本题解析:
试题分析:(1)Cu2S与Cu2O一样,铜的化合价都是+1价,所以二者最终反应均变成单质铜,化合价降低,生成2mol铜,转移电子2mol。
(2)Cu2O中加入足量稀硫酸是因为Cu2O发生了歧化反应,0价← +1 →+2价,所以有红色物质生成。Cu2O + 2H+ =" Cu" + Cu2+ +H2O
(3)要使单质铜变成硫酸铜,应该加入氧化剂把铜单质氧化,考虑不引入杂质和环保,应该选择C, H2O2 在酸性条件下可以把Cu氧化为Cu2+ ,方程式为:Cu + H2O2 + 2H+ =
本题难度:困难
5、选择题 常温下,将1.92g铜加入到100mlH2SO4和HNO3的混合液中,Cu全部溶解,放出无色气体,再向溶液中加入足量铁粉,充分反应,此时收集到气体为448ml(标准状况)的氢气。下列有关结论不正确的是(???)
A.溶解的铁粉为2.8g
B.原溶液中C(SO42-)=0.5mol/L
C.原混合溶液中C(H+)=1.2mol/L
D.原溶液中n(NO3-)=0.08mol
参考答案:D
本题解析:铜的物质的量为0.03mol,氢气的物质的量为0.02mol;发生的反应依次分别为:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
0.03? 0.08? 0.02?? 0.03
Fe?+?Cu2+=Cu+Fe2+
0.03??? 0.03
Fe?+?2H+= Fe2++H2
0.02??? 0.04?????????0.02
可知,原溶液中NO3-的物质的量为0.02mol,H+的物质的量为0.12mol,即可求出SO42―的物质的量为0.05mo
本题难度:简单
|