微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (本题共13分)甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。
步骤
| 操作
| 现象
|
Ⅰ
| 向2mL 1 mol・L-1FeCl3溶液中加入一定量的Na2SO3溶液
| 溶液由棕黄色变为红褐色,并有少量刺激性气味的气体逸出
(1)常温下,FeCl3溶液的pH_______7(填“<”、“>”或“=”)。
(2)分析红褐色产生的原因。
① 甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,请用化学平衡移动原理解释溶液呈红褐色的原因:________。
② 乙同学认为可能是发生了氧化还原反应,其中Fe3+ →Fe2+ ;请写出Fe3+ 跟SO32-反应的离子方程式
______________。
乙同学查阅资料得知:
1.Fe2+与SO32-反应生成墨绿色的絮状沉淀FeSO3;
2.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色。
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
步骤
| 操作
| 现象
| Ⅱ
| 用激光笔照射步骤I中的红褐色溶液
| 出现“丁达尔效应”
甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3。而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是________。
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
步骤
| 操作
| 现象
| Ⅲ
| 向1 mol?L-1的FeCl3溶液中通入一定量的SO2
| 溶液由黄色变为红褐色
| Ⅳ
| 用激光笔照射步骤Ⅲ中的红褐色溶液
| 没有出现“丁达尔效应”
① 经检验步骤Ⅲ中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是_________(填字母)。
a.K3[Fe(CN)6] 溶液?????????b.KSCN溶液????????c.KMnO4溶液
② 请用离子方程式和必要的文字说明步骤Ⅲ中出现红褐色的原因???????。
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
2、计算题 用黄铜矿炼铜按反应物和生成物可将总反应可以写成:
CuFeS2 + SiO2 + O2→ Cu + FeSiO3 + SO2
事实上冶炼反应是分步进行的。(1)黄铜矿在氧气作用下生成硫化亚铜和硫化亚铁;(2)硫化亚铁在氧气作用下生成氧化亚铁,并与二氧化硅反应生成矿渣;(3)硫化亚铜与氧气反应生成氧化亚铜;(4)硫化亚铜与氧化亚铜反应生成铜。
1)??写出上述各个分步反应(1,2,3,4)的化学方程式。
2)??给出总反应方程式的系数。
3)??据最新报道, 有一种叫Thibacillus ferroxidans的细菌在氧气存在下可以将黄铜矿氧化成硫酸盐。反应是在酸性溶液中发生的。试写出配平的化学方程式。
4)??最近我国学者发现,以精CuFeS2矿为原料在沸腾炉中和O2 (空气)反应, 生成物冷却后经溶解、除铁、结晶,得到CuSO4・5H2O,成本降低了许多。实验结果如下:
沸腾炉温度/℃
| 560
| 580
| 600
| 620
| 640
| 660
| 生
成
物
| 水溶性Cu/%
| 90.12
| 91.24
| 93.50
| 92.38
| 89.96
| 84.23
| 酸溶性Cu/%
| 92.00
| 93.60
| 97.08
| 97.82
| 98.16
| 98.19
| 酸溶性Fe/%
| 8.56
| 6.72
| 3.46
| 2.78
| 2.37
| 2.28
回答如下问题:
(1) ?CuFeS2和O2主要反应的方程式为:
(2) ?实际生产过程的沸腾炉温度为 600~620℃。控制反应温度的方法是:
(3) ?温度高于600~620℃生成物中水溶性Cu (%)下降的原因是:
3、选择题 下列反应的离子方程式正确的是(???)
A.硫酸铁溶液与氢氧化钡溶液反应:Fe3++3OH-====Fe(OH)3↓
B.硫化钠溶液与氯化铁溶液反应:2Fe3++3S2-====Fe2S3
C.过量的铁与很稀的硝酸溶液反应无气体放出:4Fe+10H++ ====4Fe2++3H2O+ ====4Fe2++3H2O+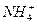
D.硫化氢气体通入氯化亚铁溶液:H2S+Fe2+====FeS↓+2H+
4、选择题 纳米是长度单位,l nm="10" -9m,当物质的颗粒达到纳米级时,会具有一些特殊的性质。例如由铜制成“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列关于“纳米铜"的叙述正确的是
A.“纳米铜”比铜片的金属性强
B.“纳 米铜”比铜片更易失去电子 米铜”比铜片更易失去电子
C.“纳米铜"比铜片的氧化性强
D.“纳米铜”的还原性与铜片相同
5、选择题 向一定量的Cu、Fe2O3的混合物中加入300 mL 1 mol・L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为?? ( )。
A.6.4 g
B.4.8 g
C.2.4 g
D.1.6 g
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772
|