��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
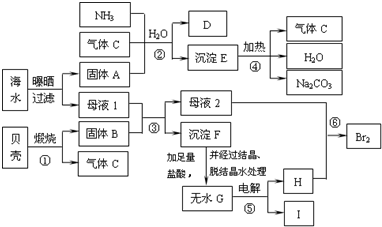
1������� ���ú�ˮ�ȿ��Ƶö��ֻ�����Ʒ����ͼ���Ժ�ˮ�����ǵ�Ϊԭ����ȡ���ֻ�����Ʒ��ת����ϵͼ������D��һ�ֵ��ʣ�HΪ����ɫ���壬I��һ�ֵ��ʣ���ԭ��K���M���������ͬ��
����д���пհף�
��1��F�Ļ�ѧʽΪ______��
��2���ڢ١���Ӧ������������ԭ��Ӧ���ǣ�����ţ�______��
��3���������̿��Եõ���Щ������Ʒ��д��3�֣�______��
��4����Hͨ��ĸҺ2���û��õ���Br2��Ũ�Ⱥ�С����Ҫ���и����������ǣ��ÿ�����Br2�������ô�����Һ���գ������ϡ�����ữ�����ɵõ�Br2��������Һ����Br2�����ӷ���ʽΪ��3Br2+3CO32-�TBrO3-+5Br-+3CO2������д����ϡ�����ữ�õ�Br2�����ӷ���ʽ______��
�ο��𰸣��������յõ���BΪ�����ƣ�CΪ������̼������AΪ�Ȼ��ƣ���Ӧ
���������
�����Ѷȣ�һ��
2������� ��ҵ���Ӻ�ˮ����ȡþ��������ͼ��ͼ��ʾ��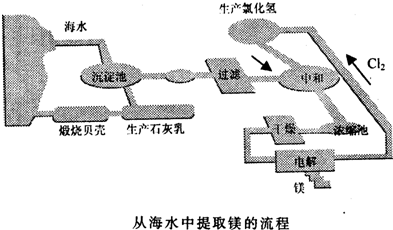
������
�ٽ����ߴ����ı������ճ���ʯ�ң�������ʯ���Ƴ�ʯ���飻
�ڽ�ʯ������뵽��ˮ�������о����˵õ�Mg��OH��2������
����Mg��OH��2�����м�������õ�MgCl2��Һ���پ������ᾧ�õ�MgCl2?6H2O��
�ܽ�MgCl2?6H2O��һ�������¼��ȵõ���ˮMgCl2��
�ݵ�����ڵ��Ȼ�þ�ɵõ�Mg��
��1����������漰�Ļ�ѧ����ʽΪ______��
��2��������е��������÷紵��ɹ��ɣ�����ʵ��������������ʱ��Ҫ����Ҫ������______��______���ƾ��ơ����Ǽܵȣ�
��3����ˮ�е�þ��Mg����ʽ���ڣ���Ʋ���ڢ۽�Mg2+ת��ΪMg��OH��2������ת��ΪMg2+��Ŀ����______��
��4��������еġ�һ��������ָ����______��Ŀ����______��
��5�����������У��ڽ��ͳɱ���������Ⱦ��������һЩ��������д������һ�㣺
��6����ͬѧ��Ϊ�������ڲ���ں����Mg��OH��2�õ�MgO���ٵ�����ڵ�MgO�ƽ���þ���Լ�ʵ�鲽�裬����ʵ��ļ�Լ��ԭ�����Ƿ�ͬ���ͬѧ�Ĺ۵�______���ͬ�⡱��ͬ�⡱��������Ϊ______��
�ο��𰸣���1��̼��Ƽ��ȷֽ���������ƺͶ�����̼�������ƺ�ˮ��Ӧ����
���������
�����Ѷȣ�һ��
3������� þ��һ�����ʻ��á���;�㷺�Ľ������о�þ��ұ�����ʶ������������������ش�
��һ��Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ���֪�Ӻ�ˮ������þ����Ҫ������ͼ��
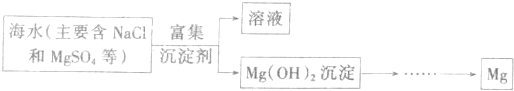
ѧ������������������������⣺
��1���Ӻ�ˮ����ȡþ�Ĺ��������ʵ�ֶ�þ�ĸ�����
ѧ��1�Ĺ۵㣺ֱ������ˮ�м����������
ѧ��2�Ĺ۵㣺���¼���������ˮ���ټ����������
ѧ��3�Ĺ۵㣺����������ˮɹ�κ�ʣ�����Һ�������������
������������ѧ������Ĺ۵��Ƿ��������ǡ���������������������ɣ�
| �۵� | �Ƿ���ȷ | ��������
ѧ��1
��
______
ѧ��2
______
______
ѧ��3
______
______
��2���Ӻ�ˮ����þ�Ĺ��������ʵ�ֶ�þ�ķ��룿
�ٹ��������ó�����������ԭ��Ҳ��Դ�ں�����ó�������______���ѧʽ����
���Դӽ�Լ��Դ����߽���þ�Ĵ��ȷ��������������˵�ұ��þ�ķ�����______����ѡ����ĸ����
A��Mg��OH��2��
MgO���
2800��
Mg
B��Mg��OH��2��
MgOC���
1352��
Mg
C��Mg��OH��2�ٹ�������
�ڡ�
��ˮMgCl2���
714��
Mg
D��Mg��OH��2����
MgCl2��Һ���ý���
Mg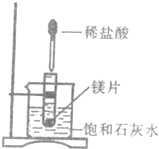
������Ϊ���о�þ�����ʣ����ù�ҵ�ƵõĴ�����þ����ͼ��ʾʵ�飮���Թܷ���ʢ��25�汥��ʯ��ˮ���ձ��У�Ȼ�����Թ��з���þƬ�����õιܵ���һ�������ᣮ��ش�
��1��ʵ���й۲쵽��������
��______����______����______��
��2���ձ��в�����Ӧ�����ԭ��Ϊ______��
�ο��𰸣���һ����1��ѧ��1���������Ȼ�þŨ�Ⱥ�С������Һ�м���ʯ����
���������
�����Ѷȣ�һ��
4������� ��1����Դ�ǵ�����ᷢչ������֧��֮һ����Ȼ����һ�ָ�Ч���ͺġ���ȾС�������Դ����Ҫ�ɷ�Ϊ���飬����ȼ�յĻ�ѧ����ʽΪ��__________ �� ��״���£�11.2L����ȼ��ʱ��ת�Ƶ��ӵ����ʵ���Ϊ__________ mol��? ������ͼ���������ѭ����̫��������ת��Ϊ _________�ܡ�
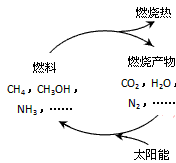
��2�������ĸ�ʴ����dz��ձ飬�绯ѧ��ʴ����ɸ�����ʴ����Ҫԭ��ijͬѧ����ͼ���и�����ʴ��ģ�⣬���ĵ缫��ӦʽΪ________ �� �����ĵ缫��ӦʽΪ _________�� ����ʾ���绯ѧ���ܷ�ӦʽΪ2Fe+2H2O+O2==2Fe(OH)2��

��3����ˮ��ѧ��Դ�Ŀ������þ�����Ҫ����������ã���ͼ�Ǻ�������ȡ���ʾ��ͼ��

�����ٵ�������_________ ����Ӧ�ڵ����ӷ���ʽ��__________ �����������в������Լ��۵���____________ ��
A���Ҵ�
B����
C������
D�����Ȼ�̼
�ο��𰸣���1��CH4 +2O2![]() ��������� ���������
�����Ѷȣ�һ��
5��ѡ���� ����������ȷ���� [???? ]
A�����Ӵ�������H2SO4ʱ���������εķ�Ӧԭ��Ϊ2SO2(g)+O2(g)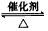 2SO3(g) ��H<0 2SO3(g) ��H<0
B����ˮ��þ����Ҫ����Ϊ
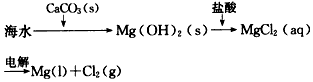
C����ͨˮ�����Ҫ�ɷ��ǹ����
D���������Ҫ�ɷ�������������
�ο��𰸣�AC
���������
�����Ѷȣ���
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772
|