微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (17分)根据下表部分短周期元素的性质或原子结构,用化学用语回答下列问题。
元素编号
| 元素性质或原子结构
|
R
| 元素所处的周期数、主族序数、原子序数均相等
|
T
| 最外层电子数是次外层电子数的2倍
|
X
| 元素最高正价+7价
|
Y
| 第三周期金属元素中原子半径最小
|
Z
| 常温下单质为双原子分子,其氢化物水溶液呈碱性
(1)写出元素T的原子结构示意图??????????????????;元素Z单质的电子式??????????????????;写出X在周期表中的位置??????????????????????????? ;元素T的最高价氧化物的结构式????????.
(2)探寻物质的性质差异是学习的重要方法之一。上述T、X、Y、Z四 种元素最高价氧化物的水化物的酸性最强的是??????????????????(填化学式),其中化学性质明显不同于其他三种化合物的 种元素最高价氧化物的水化物的酸性最强的是??????????????????(填化学式),其中化学性质明显不同于其他三种化合物的
是??????????????????(填化学式),理由是????????????????????????????????????。
(3)写出R、T、X、三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的化学式???????????????
(4)由表中元素形成的常见物质A、B、C、D、E可发生以下反应:
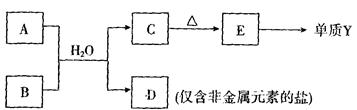
A溶液与B溶液(呈碱性)反应的离子方程式为?????????????????????????????????。
D中含有化学键的类型是?????????????????????,属于??????(填“离子”或“共价”)化合物。
2、填空题 (10分)有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复) 提示:CH3COONH4溶液为中性
阳离子
| Na+、Ba2+、NH4+
| 阴离子
| CH3COO-、Cl-、OH-、SO42-
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A是______ ,B是_______ ,C是_______ ,D是________ 。
(2)用离子方程式表示A的水溶液显碱性的原因________________________________。
(3)25℃时,0.1mol・L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3・H2O)= _______(用含a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为____________????????????????????????????_______。
3、判断题 有一结晶水合物X・6H2O,其水溶液为浅绿色,可发生如下的转化(部分反应物、生成物从略)。其中B、D、E、F均为无色气体,G为难溶于水的红褐色固体。在A溶液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀。
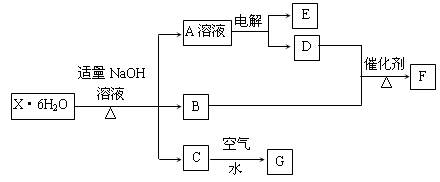
请回答下列问题:
⑴指出C→G的基本反应类型:_________反应。
⑵用惰性电极电解溶液A时得到E的电极反应式为____________________________。
⑶B与D反应生成F的化学方程式为__________________________________。
⑷该晶体水合物的化学式为_________________________________。
(5)在空气中灼烧X・6H2O晶体能否得到X无水盐?????(填:能或否),理由是????????????。
4、填空题 (12分)元素X、Y、Z、M、Q均为短周期主族元素,且原子序数依次增大。已知元素Y最高价氧化物对应水化物与它的氢化物反应能生成一种盐;Z原子最外层电子数与核外电子总数之比为3:4;M可与Z形成阴、阳离子个数比为1:2的两种化合物,Q原子的最外层电子数与次外电子数之比为3:4,YX3常温下为气体。
(1)化合物A、B由X、Z、M、Q四种元素中的三种组成的强电解质,且A属于碱,B属于盐,组成元素的原子数目之比均为1:1:1,则化合物A的化学式为????????,B的化学式是???????????。
(2)Se是人体必备的微量元素,与Q同一主族。该族二至五周期元素单质分别与H2反应生成1mol 气态氢化物的反应热如下,表示生成1 mol哂化氢反应热(△H)的是?????(填字母代号)。
A.+99.7kJ・mol-1???????????????????????????????????????????????????????????????????????????????????????B.+29.7 kJ・mol-1
C.-20.6 kJ・mol-1???????????????????????????????????????????????????????????????????????????????????????D.-241.8 kJ・mol-1
(3)X与Z、X与Q均可形成18电子分子甲和乙,写出甲、乙两种分子在水溶液中反
应生成Q单质的化学方程式??????????。X和Y也可形成18电子分子丙,它通常是一种液态火箭燃料。25℃、常压下,3.2g丙在氧气中完全燃烧放出热量为62.4kJ,请写出丙完全燃烧的热化学反应方程式????????????????????????。
(4)X、Y两种元素形成的离子化合物的电子式为?????????????。
5、填空题 有三种固体物质和五种溶液:固体是铁粉、铜粉、氢氧化铜;溶液是CuSO4溶液、NaOH溶液、FeSO4溶液、H2SO4溶液、Na2SO4溶液.它们中的几种物质在常温下相互转化关系如下:
(1)溶液A+溶液C→固体甲+溶液D
(2)固体乙+溶液B→溶液E+氢气
(3)固体甲+溶液B→溶液C+水
试推断溶液中A、B、C、D、E及固体甲、乙、丙的名称.
A、______??B、______????乙、______?丙、______
写出反应(1)(3)的方程式:
(1)______(3)______.
|
|