微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (15分)
请设计实验:用MnO2与浓盐酸制备纯净、干燥的Cl2,其他药品与试剂任选。
(1)写出该反应的化学方程式?????????????。
 ?(2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必
?(2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必 画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如
画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如 下:
下:
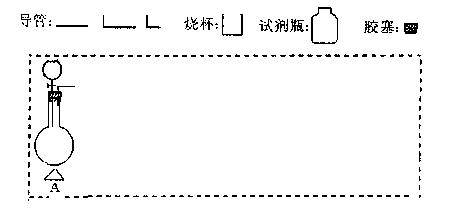
(3)根据方框中的装置图,完成下表(若无需填写,则在表格中写“无”)
仪器符号
| 仪器中所加物质
| 作用
|
A
| MnO2、浓盐酸
| MnO2与浓盐酸生成Cl2
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
??(4)KMnO2与浓盐酸在常温下反应也可以得到Cl2,请写出该反应的离子方程式????。
(5)请写出Cl2在工业、农业、医疗、卫生等方面的用途??????????。(写出两种即可)
(6)将Cl2与SO4分别通人品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法。
参考答案:
(1)MnO2+4HCl(浓)![]()
本题解析:略
本题难度:简单
2、实验题 (8分)用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③稀释、降温;④转移、洗涤;⑤定容、摇匀。回答下列问题
(1)所需浓硫酸的体积是?????? ??; ??;
(2)第⑤步实验的具体操作是???????????????????????????????????????????????????????????????????????????????????????
??????????????????????????????????? ??????????????????????????。 ??????????????????????????。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏洗涤后残留有少量的水???????????????
B.所用过的烧杯、玻璃棒未洗涤?????????????????
C.定容时俯视溶液的液面????????????????????
参考答案:(1)16.7ml (2分)??
(2)继续向容量瓶注
本题解析:略
本题难度:一般
3、实验题 (12分)全世界每年被腐蚀损耗的钢铁约占全年钢铁产量的1/10,而在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因。
(1)在潮湿空气中,钢铁发生吸氧腐蚀转化为Fe(OH)2的电池反应方程式为??? ▲???。
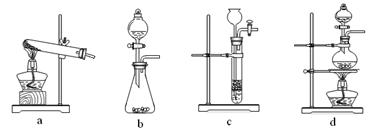
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是??? ▲???。(填字母) CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是??? ▲???。(填字母)
(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3・nH2O和Fe两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
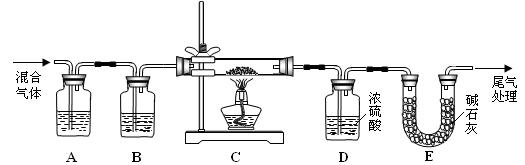
①为得到干燥、纯净的CO气,洗气瓶A、B中盛放的试剂分别是??? ▲???、??? ▲???。
②在点燃酒精灯之前应 进行的操作是:(a)检查装置气密性;(b)?? ▲???。 进行的操作是:(a)检查装置气密性;(b)?? ▲???。
③准确称量样品的质量10.00 g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =??? ▲??。
④在本实验中,下列情况会使测定结果n偏大的是??? ▲???。(填字母)
a.缺少洗气瓶B?? b.缺少装置E?? c.反应后固体是铁和少量Fe2O3・nH2O
参考答案:共12分。
(1)2Fe + O2 本题解析:略 本题解析:略
本题难度:简单
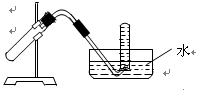
4、选择题 右图装置可用于?????
A.加热NaHCO3固体制CO2
B.Cu和稀HNO3反应制NO
C.NH4Cl与浓Ca(OH)2溶液反应制NH3
D.Cu和浓HNO3反应制NO2
参考答案:B
本题解析:装置中看出为固液和液液反应,排水法收集;A、固体加热,试管向下倾斜;B、可以;C、氨气不能使用排水法;D、二氧化氮不能使用排水法。
本题难度:简单
5、实验题 单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
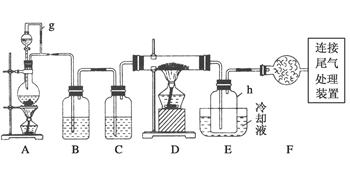
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物质
| SiCl4
| BCl3
| AlCl3
| FeCl3
| PCl5
| 沸点/℃
| 57.7
| 12.8
| ―
| 315
| ―
| 熔点/℃
| -70.0
| -107.2
| ―
| ―
| ―
| 升华温度/℃
| ―
| ―
| 180
| 300
| 162
请回答下列问题:
(1)写出装置A中发生反应的离子方程式______________________。
(2)装置A中g管的作用是________;装置C中的试剂是________;装置E中的h瓶需要冷却的理由是__________________________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是________(填写元素符号)。
参考答案:(1)MnO2+4H++2Cl-△Mn2++Cl2↑+2H2
本题解析:略
本题难度:一般
|
|