微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)实验室用固体烧碱配制480mL 1mol/L NaOH溶液。
(1)需称量 ??????g的烧碱固体,固体应放在??????中称量。
(2)配制过程中,不需要使用的仪器是(填写代号 )??????????????????。
)??????????????????。
A?烧杯??? B?量筒??????? C ? 1000mL容量瓶???? D?玻璃棒???
? 1000mL容量瓶???? D?玻璃棒???
E?漏斗??? F?胶头滴管??? G? 500mL试剂瓶
(3)根据实验的实际需要和(2)中列出的仪器判断,完成实验还缺少的仪器是???????????????????????????;
(4)在定容的过程中,后期加入少量水的做法是??????。
2、实验题 K3[Fe(C2O4)3]・3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应的化学方程式为:Fe+H2SO4 FeSO4+H2↑
FeSO4+H2↑
FeSO4+H2C2O4+2H2O FeC2O4・2H2O↓+H2SO4
FeC2O4・2H2O↓+H2SO4
2FeC2O4・2H2O+H2O2+H2C2O4+3K2C2O4 2K3[Fe(C2O4)3]+6H2O
2K3[Fe(C2O4)3]+6H2O
2Mn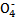 +5C2
+5C2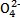 +16H+
+16H+ 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
回答下列问题:
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是 。?

(2)在将Fe2+氧化的过程中,需控制溶液温度不高于40 ℃,理由是 ;得到K3[Fe(C2O4)3]溶液后,加入乙醇的理由是 。?
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量, ②置于烘箱中脱结晶水,③冷却,④称量,⑤ (叙述此步操作),⑥计算。步骤③若未在干燥器中进行,测得的晶体中所含结晶水含量 (填“偏高”“偏低”或“无影响”);步骤⑤的目的是 。?
(4)晶体中C2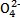 含量的测定可用酸性KMnO4标准溶液滴定。称取三草酸合铁(Ⅲ)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0.010 0 mol・L-1酸化的高锰酸钾溶液进行滴定。
含量的测定可用酸性KMnO4标准溶液滴定。称取三草酸合铁(Ⅲ)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0.010 0 mol・L-1酸化的高锰酸钾溶液进行滴定。
①下列操作及说法正确的是 。?
A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量标准液,使尖嘴充满液体
C.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴
②有同学认为该滴定过程不需要指示剂,那么滴定终点的现象为 ,若达到滴定终点消耗高锰酸钾溶液V mL,那么晶体中所含C2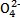 的质量分数为 (用含V、m的式子表示)。?
的质量分数为 (用含V、m的式子表示)。?
3、实验题 (20分)(I) 下图甲和乙是某学校王老师制备NH3 并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g固体氯化铵装入试管底部,再快速称取2g氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL 浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.
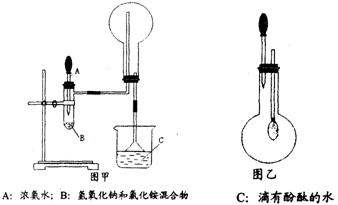
将上述中收满NH3 的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O ,此时小气球系在玻璃棒上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该化学方程式为:__________________________________________________________
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是__________。
①在NH3 ・ H2O 中有平衡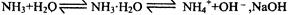 使平衡向左移动
使平衡向左移动
②在NH3・ H2O 中有平衡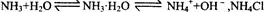 使平衡向左移动
使平衡向左移动
③Na0H 溶于水时放热,使体系的温度升高,NH3的溶解度减小
④NH4Cl与NaOH 在此情况下可反应生成NH3,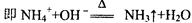
⑤NH4Cl 会分解释放出NH3
(3)图甲中的NH4Cl 与NaOH 固体混合物能否用CaO 固体代替????(填”能”与”不能”)
(4)如何判断图甲中烧瓶己收满NH3 ?_____________________________________________
(5)图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是???????????????它说明了NH3
????????????????
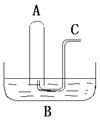
(Ⅱ)如上图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL,则原混合气体中NO2和NO的物质的量之比为?????????????????
通过导气管C往余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是:
___________________________________________________??????????????????????????????????????????????????????????
有关反应的化学方程式为:___________________________________________
当试管A中充满气体时停止通入氧气,然后将试管取出水槽,则共通入氧气的体积为???? ________mL,水槽B中溶液的物质的量浓度为???????mol・L-1(设溶液的体积仍为500 mL)
4、实验题 实验室用二氧化锰和浓盐酸制取氯气
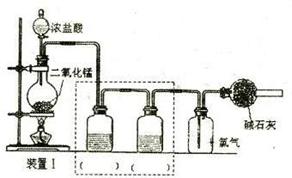
(1)实验室制取氯气的离子方程式?????????????
(2)二氧化锰放在?????????????浓盐酸放在?????????????(填仪器名称)
(3)实验室制取氯气以前,首先应该进行???????除了向上排气法收集氯气外,还可以用???????????????????????????收集。
(4)图中两个洗气瓶放置的试液依次是?????????????,?????????????图中错误是??????????
(5)碱石灰的作用是?????????????
(6)制取标准状况下11.2L氯气转移电子?????摩尔,被氧化的氯化氢是?????摩尔。
5、选择题 不能用排空气法收集的气体是( )
A.CO2
B.NO2
C.NO
D.H2