��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� С��ͬѧ������ͼ��ʾװ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У����밴Ҫ����գ�
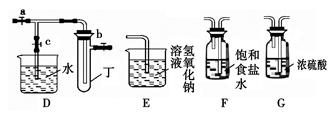
��1�����ö������̺�Ũ������ȡ�����������������Ҫ�õ�����������˳��Ϊ��A��?????????????????????????????????????��
��2������Bװ�ÿ���ȡ��������????????????????����2�֣���
��3��B��D��Eװ����������B��ʢװ����Ũ�����ͭƬ�������п����ϰ��ϣ������Ƶ�NO2�������й�ʵ�顣B�з�����Ӧ�Ļ�ѧ����ʽΪ??????????????????????????????????????????????������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ��?????���ٴ�ֹˮ��?????��ʹ�ձ��е�ˮ�����Թܶ��IJ�����??????????????????????????????????��
�ο��𰸣���1��A��F��G��C��E???��2��H2��CO2��H2S�ȣ�
���������
�����������1��ʵ��װ�õ�����˳��Ϊ������װ�á�����װ�á��ռ�װ�á�β������װ�ã���Ϊ����ʳ��ˮ����ˮ��Ũ��������ˮ�ԣ����������ӱ���ʳ��ˮװ�ú�����Ũ����װ�ã���2��Bװ��Ϊ��״������ˮ�Ĺ����Һ�巴Ӧ��ȡ�����װ�ã��ҷ�Ӧ����Ҫ���ȣ����ɵ����岻������ˮ����ѧ��ѧ�г������У�H2��CO2��H2S?�ȣ���3��Ũ�������ǿ�����ԣ���ͭ��Ӧ���ɶ����������壬��Ӧ�Ļ�ѧ����ʽΪCu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��Ũ������ͭ��Ӧ���ɵĶ��������ռ����Թܶ��У�װ����֤NO2��ˮ�ķ�Ӧ��Ҫ�ȹر�a��b��Ȼ�����ȷ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У��ʴ�Ϊ��a��b��c��˫�ֽ��գ����ȣ��Թܶ���ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У�2��ˮ�ķ�Ӧ
�����Ѷȣ�һ��
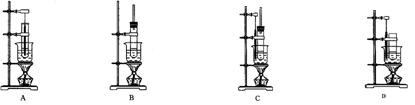
2��ѡ���� ��������ʵ��װ�ã�����ͼ��ʾ��Ҫ�Ʊ���������Ӧѡ��???????????
 ????????
????????
�ο��𰸣�B
�����������
�����Ѷȣ���
3��ѡ���� ����˵����ȷ����????????????????????????????????????????????????????????????????????????????????????????��???��
A����25g CuSO4��5H2O����1Lˮ�У������Ƴ�0��1 mol��L-1CuSO4��Һ
B������������ȥ�������������л��е�������
C���������ſ������ռ�NH��������ʪ�����ɫʯ����ֽ����NH���Ƿ��ռ�����
D������Ȳʱ���ñ���ʳ��ˮ����ˮ��Ϊ�˼�����ʯ��ˮ�ķ�Ӧ����
�ο��𰸣�D
���������ѡ��AӦ��25g CuSO4��5H2O����ˮ�У�������1L��Һ��ѡ��BӦ������������ѡ��CӦ����ʪ��ĺ�ɫʯ����ֽ����NH���Ƿ��ռ����ˡ�
�����Ѷȣ���
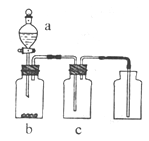
4��ѡ���� ����ͼװ����ȡ���ᴿ���ռ����е��������壨a��b��c��ʾ��Ӧ�����м�����Լ��������п��е���???????????? (?? )
?
| ����
| a
| b
| C
|
A
| NO2
| Ũ����
| ͭƬ
| NaOH��Һ
|
B
| SO2
| Ũ����
| ͭƬ
| ����KMnO4��Һ
|
C
| CO2
| ϡ����
| Na2CO3����
| Ũ����
|
D
| NH3
| Ũ��ˮ
| ��ʯ��
| Ũ����
�ο��𰸣�C
���������A����NO2������NaOH��Һ����ᱻ���գ�B����SO2��Ҫ����������D��NH3������Ũ�����������յ�NH3
�����Ѷȣ�һ��
5��ʵ���� �ؾ�ʯ�����Ҫ�ɷ�Ϊ���ᱵ�����������ᱵ���ܹ�ҽ���������͡����ڶ�ijЩ�������ٽ���X������ʱ���á����ǿ�����ˮ���Ρ��������ؾ�ʯ�������ᱵ������������£�
 ?��1��д������ٵĻ�ѧ��Ӧ����ʽ????????????���÷�Ӧ�������������????????????��????????????����;�� ?��1��д������ٵĻ�ѧ��Ӧ����ʽ????????????���÷�Ӧ�������������????????????��????????????����;��
��2��Ϊ���Тڷ�Ӧ��Ҫ���������Һ�����õķ�����??????????????????���ڴ�֮ǰҪ����Һ�е�������Ba��OH��2��Һ����������????????????��
��3����B�����ڸ����������п�ѭ��ʹ�ã���۷�Ӧ�Ļ�ѧ����ʽ�ǣ�????????????????????????��
��4����������ڷ�Ӧ�������г��ж������壬�ɲ��øı䷴Ӧ��ķ���ʹ�������������ڷ�Ӧ�Ļ�ѧ����ʽ�ǣ�?????????????????????????????????����ʱ��ҪB���ʻ���ѭ��ʹ�ã���CΪ????????????��д��ѧʽ����
��5��BaSO4����Ϊ����????????????��????????????�����ʶ������������͡��ġ�
�ο��𰸣�
��1��BaSO4+4C ��������� ���������
���⿼��������ʵ�顣��1����Ӧ��Ϊ���ᱵ��̼�������������������������ΪCO��CO������Ϊȼ�ϡ���ԭ���ȣ���2����ΪS2������ˮ�ⷴӦ��S2����H2O HS����OH�������Լ���Ba��OH��2��Һ��Ŀ����������ˮ�⣻��3���������ᷴӦ����H2S��BaCl2��A����ΪBaCl2����ΪB���ʿ���ѭ�����ã���C�����ᣬ����B�����ᣬ�������⣻��4���������ΪCuC12��ԭ����CuS������ˮ���ᡣ HS����OH�������Լ���Ba��OH��2��Һ��Ŀ����������ˮ�⣻��3���������ᷴӦ����H2S��BaCl2��A����ΪBaCl2����ΪB���ʿ���ѭ�����ã���C�����ᣬ����B�����ᣬ�������⣻��4���������ΪCuC12��ԭ����CuS������ˮ���ᡣ
�����Ѷȣ�һ��
|