微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铝在人体中积累可使人慢慢中毒,1989年世界卫生组织正式将铝确定为食品污染源之一并加以控制。铝在下列场合使用必须加以控制的是????(???)
①制铝锭,②制易拉罐,③制电线电缆,④制牙膏皮,⑤用明矾净水,⑥制炊具,⑦用明矾和小苏打做食品膨化剂,⑧用请氢氧化铝[Al(OH)3]制成药片制胃病,⑨制防锈油漆
A.①②④⑤⑥⑦⑧
B.②⑤⑥⑦⑨
C.②④⑤⑥⑦⑧
D.③④⑤⑥⑦⑧
参考答案:C
本题解析:本题要注意题干要求世界卫生组织正式将铝确定为食品污染源之一并加以控制,所有要找到和食品有接触关系的铝制品,所以可以得出符合的项目有②④⑤⑥⑦⑧,正确答案为C。
本题难度:一般
2、选择题 工业上制造镁粉是将镁蒸气在气体中冷却.可作为冷却气体的是( )
①空气??? ②CO2 ?? ? ③Ar??? ?④H2???? ?⑤N2.
A.①②
B.②③
C.③④
D.④⑤
参考答案:C
本题解析:
本题难度:简单
3、填空题 LiBH4为近年来储氢材料领域的研究热点。
(1)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L H2(标准状况)时,转移电子的物质的量为????mol。
(2)下图是2LiBH4/MgH2体系放氢焓变示意图,则:
Mg(s)+2B(s)=MgB2(s) △H=????????。

(3)采用球磨法制备Al与LiBH4的复合材料,并对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是????(填字母)。

a.25℃时,纯铝与水不反应
b.25℃时,纯LiBH4与水反应产生氢气
c.25℃时,Al-LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。
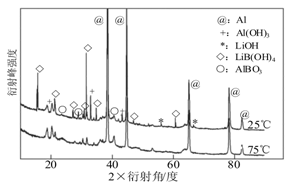
从图中分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是???????????(填化学式),产生Al(OH)3的化学方程式为?????????????????。
(4)如图是直接硼氢化钠-过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH????????(填“增大”、“减小”或“不变”),负极的电极反应式为????????????????????????。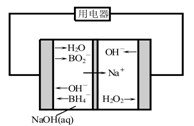
参考答案:
(1)2(2分)
(2)-93 kJ・mol-
本题解析:
试题分析:(1)LiBH4中氢元素化合价为-1价,生成1mol氢气电子转移2mol;(2)能量由上到下分别为1、2、3、4,则该反应的焓变为-(1+3-2-4)= -93 kJ・mol-1;(3)①a、图中当全为铝时气体为0,故纯铝与水不反应,正确;b、f线代表纯LiBH4与水反应产生氢气,正确;c、当材料含LiBH4为25%时(d线),产生氢气的量最多,错误。②由图12得出反应后已没有LiBH4,但存在大量铝,故其完全反应,;铝部分反应(有氢氧化铝等铝的产物);(4)右室双氧水得到电子为正极,电
本题难度:一般
4、填空题 某化学兴趣小组用铝土矿(主要成分为A12 O3,还含有SiO2及铁的氧化物)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
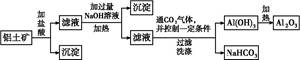
(1)在过滤操作中,除烧杯、玻璃棒外,还需用到的玻璃仪器有???????????;洗涤沉淀的操作是????????????????????????????????????????????????????????????????????????。
(2)实验室制备氢氧化铝的方案有多种。现提供铝屑、氢氧化钠溶液、稀硫酸三种药品,若制备等量的氢氧化铝,请你从药品用量最少的角度出发,设计出最佳实验方案(方案不必给出),写出此方案中发生反应的离子方程式:???????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????,此方案中所用药品的物质的量之比是:n(Al)∶n(H2SO4)∶n(NaOH) =???????。
(3)兴趣小组欲对铝土矿中铁元素的价态进行探究:取少量固体,加入过量稀硝酸,加热溶解;取少许溶液滴加KSCN溶液后出现红色。由此得出铁元素的价态为+3的结论。请指出该结论是否合理并说明理由???????????????????????????????????????????????????????。
参考答案:(1)普通漏斗??向漏斗里加入蒸馏水,使水面浸没沉淀,等水自
本题解析:(1)过滤装置中还缺少普通漏斗。洗涤时,向过滤器中加蒸馏水浸没沉淀,等水自然流下后,重复2~3次,可洗涤其表面吸附的离子。(2)制备氢氧化铝有三种途径:铝与硫酸反应生成硫酸铝,硫酸铝与氢氧化钠反应得氢氧化铝沉淀;铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠再与硫酸反应得氢氧化铝;将铝按物质的量之比1∶3转化为Al3+、AlO2-,利用Al3+和AlO2-的相互促进水解制取氢氧化铝。写出方程式观察第三种方法最节约原料。(3)从实验现象来看,只能说明铝土矿中含有铁元素,但是铁的价态不一定是+3价,因为硝酸具有强的氧
本题难度:一般
5、填空题 (12分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。
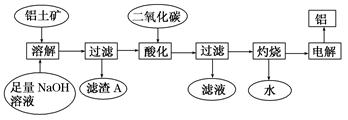
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式????????????????????????????????????????????????,滤渣A的主要成分为??????????????????????。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为???_______??。
(3)电解氧化铝,每生成1molAl时,生成?????????g氧气。
参考答案:(12分)
(1) 2 OH―+Al2O3="=" 2A
本题解析:(1)铝土矿的主要成分是Al2O3,Al2O3与NaOH反应,生成盐和水,则剩下Fe2O3没有反应,过滤后成为滤渣。(2)Na AlO2酸化之后是“过滤”,即酸化须得沉淀Al(OH)3。Al(OH)3溶于强酸而不溶于弱酸,此题要制备铝,就要提高铝的转化率。所以须用弱酸。过量的二氧化碳反应生成酸式盐。(3)根据电子守恒,生成1molAl,转移3mol电子,同时生成氧气3/4mol,即24克
本题难度:一般