微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 12.0 g某液态有机化合物A完全燃烧后,生成14.4 g H2O和26.4 gCO2。测得有机化合物A的蒸气对H2的相对密度是30,求:

(1)有机物A的分子式 。
(2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为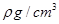 )的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1 molA分子中有x mol氢原子能跟金属钠反应,则x的计算式为 (可以不化简)。
)的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1 molA分子中有x mol氢原子能跟金属钠反应,则x的计算式为 (可以不化简)。
参考答案:(1)C3H8O(2分)
本题解析:
试题分析:(1)根据阿伏加德罗定律可知,在相同条件下气体的相对分子质量之比等于密度之比,该化合物的蒸气对氢气的相对密度为30,则该化合物的相对分子质量为30×2=60,则12g有机物的物质的量是
12g÷60g/mol=0.2mol
n(H2O)=14.4g÷18/mol=0.8mol
n(CO2)=26.4g÷44/mol=0.6mol
所以12.0g有机物中含有:m(C)=0.6mol×12g/mol=7.2g
m(H)=2×0.8mol×1g/mol=1.6g
则m(O)==12.0g-7.2g-1.6g=3.2g
n(O)=3.2g÷16g/mol=0.2mol
所以有机物中含有:N(C)=3,N(H)=8,N(O)=1
则有机物分子式为C3H8O
(2)amL(密度为ρg/cm3)的有机物A的质量为:m=aρg
物质的量为:aρg÷60g/mol= mol
mol
量筒液面读数为bml,即生成氢气的体积为bml
则n(H2)=0.001bL÷22.4L/mol
则C3H8O+xNa C3H(8-x)ONa+0.5xH2
C3H(8-x)ONa+0.5xH2
1 0.5x
 mol
mol 
解之得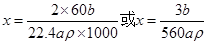
考点:考查有机物分子式的确定
点评:该题是基础性试题的考查,试题贴近教材,紧扣基础,有利于调动学生的学习兴趣和学习积极性,难度不大。该题的关键是根据原子守恒法来解答,有助于培养学生的规范答题能力。
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA
B.常温常压下,18 g H2O中含有的原子总数为3NA
C.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA
D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA
参考答案:B
本题解析:A项,Cl2溶于水为可逆反应,不能完全与水反应,错;B项,不论何条件,1 mol H2O均含有3 mol原子,正确;C项,标准状况下,CH3CH2OH为液态,不适用于气体摩尔体积,错;D项,非标准状况,无法计算出气体的物质的量,错。
本题难度:一般
3、选择题 下列叙述中正确的是( ? )
A.每摩尔物质约含有6.02×1023个粒子
B.氧气的摩尔质量是32 g
C.1 mol任何气体的气体摩尔体积都约是22.4 L・mol-1
D.1 mol・L-1硫酸溶液的含义是指1 L水中含有l mol硫酸
参考答案:A
本题解析:
试题分析:A.每摩尔物质约含有6.02×1023个粒子,A选项正确。
B.摩尔质量的单位是g/mol;应说氧气的摩尔质量是32 g/mol;
C.应强调是在标准状况下。1 mol任何气体的气体摩尔体积都约是22.4 L・mol-1;
D.应说成:1 mol・L-1硫酸溶液的含义是指1 L溶液中含有l mol硫酸
点评:要熟练掌握物质的量、摩尔质量、气体摩尔体积及物质的量浓度的概念,这些是高考的常考点。
本题难度:简单
4、填空题 将质量比为15:7的NO和N2混合,则混合气体中NO和N2的物质的量之比为______;氧原子和氮原子的个数之比为______;22g该混合气体在标准状况下的体积为______L.
参考答案:质量比为15:7的NO和N2混合,则混合气体中NO和N2的物
本题解析:
本题难度:简单
5、填空题 环境污染中除了有害气体产生的空气污染外,重金属离子在溶液中引起的水体污染也相当严重.近年来城市汽车拥有量呈较快增长趋势,汽车尾气的主要有害成分一氧化碳和氮氧化物加重了城市空气污染.研究NO2、SO2、CO等大气污染气体的处理及研究重金属离子水污染的处理具有非常重要的意义.
(1)一定条件下,NO2与SO2反应生成SO3和NO两种气体.将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,若测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=??????.
(2)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例).
已知:NO不能与Na2CO3溶液反应.
NO+NO2+Na2CO3=2NaNO2+CO2;2NO2+Na2CO3=NaNO2+NaNO3+CO2
用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则混合气体中NO和NO2的体积比为???????????.
(3)如图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质.A为电池的??????极(选填“正”或“负”).写出B极电极反应式??????????????????????????.

 (4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.
(4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.
已知: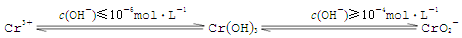
在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.用离子方程式表示溶液pH不能超过10的原因?????????????????????????????.
(5)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中.
CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示.则B点时剩余固体的成分是?????????????(填化学式).
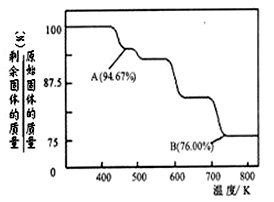
参考答案:
(1)2.67或8/3(2分)
(2)1∶7(
本题解析:
试题分析:(1)设原来NO2、SO2的体积分别是1L、2L,参加反应的二氧化氮的体积是x,
NO2?+ SO2 
 本题难度:困难
本题难度:困难