微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NA表示阿伏加德罗常数,下列叙述正确的是
A.2.4g金属镁变为镁离子时失去的电子数为0.2NA
B.1 mol・L-1KCl溶液中含有Cl-的个数为NA
C.在常温常压下,18 g水中含有的分子数为NA
D.在常温常压下,11.2L N2含有的分子数为0.5NA
参考答案:AC
本题解析:
试题分析:2.4g金属镁的物质的量为0.1mol, ,所以失去的电子0.2mol,故A正确;没有溶液的体积,不能求溶质的物质的量,故B错误;18 g水的物质的量为1mol,所以含有的分子数为NA,故C正确;标准状况下,11.2L N2含有的分子数为0.5NA,故D错误。
,所以失去的电子0.2mol,故A正确;没有溶液的体积,不能求溶质的物质的量,故B错误;18 g水的物质的量为1mol,所以含有的分子数为NA,故C正确;标准状况下,11.2L N2含有的分子数为0.5NA,故D错误。
考点:本题考查阿伏伽德罗常数。
本题难度:一般
2、计算题 (6分)用31.6g KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸,反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
⑴该盐酸的物质的量浓度为 ?
⑵有 mol HCl被氧化?
⑶产生的Cl 2在标准状况下的体积为 ?
参考答案:(1)11.9mol/L
本题解析:考查物质的量的有关计算。
(1)根据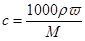 可知,盐酸的浓度是
可知,盐酸的浓度是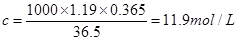 。
。
(2)31.6g KMnO4的物质的量是31.6g÷158g/mol=0.2mol,得到0.2mol×5=1.0mol电子。氯元素的化合价从-1价升高到0价,所以被氧化的盐酸的物质的量是1mol。
(3)根据方程式可知生成氯气的物质的量是0.5mol,所以在标准状况下的体积是0.5mol×22.4L/mol=11.2L。
本题难度:一般
3、选择题 某同学需配制100 g 12%的NaOH溶液来制作“叶脉书签”。在配制溶液过程中,下列做法正确的是 [???? ]
A.称量前发现指针向右偏,应调节螺母至平衡
B.在托盘上垫纸称量12g NaOH固体
C.用100mL量筒量取88 mL水
D.用药匙搅拌,加速NaOH溶解
参考答案:AC
本题解析:
本题难度:简单
4、选择题 Fe和Fe2O3的混合物,加入200mL 5mol・L-1的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中Fe2+的物质的量浓度为(假设反应后溶液体积仍为200mL):( )
A.2.5mol・L-1
B.l mol・L-1
C.2mol・L-1
D.5mol・L-1
参考答案::A
本题解析:
试题分析:其中加入KSCN溶液,未见血红色说明溶液中只含有Fe2+不含有Fe3+溶质全部为FeCl2,
盐酸的物质的量为0.2x5=1mol根据Cl元素守恒可知含有 0.5mol FeCl2
则FeCl2浓度为0.5/0.2=2.5mol?L-1,故选A
考点:铁和铁的化合物的性质,化学方程式的相关计算。
点评:若用守恒法来考虑和计算的话,不但思路清楚,而且解题简单。
本题难度:一般
5、选择题 列物质按质量由大到小的顺序排列正确的是??????( ???)
①2个铝原子?? ② 1×10-2mol铜? ③6个水分子? ④ 0.5g二氧化碳
⑤ 1×10-3mol臭氧(O3)
A ④>②>⑤? B②>①>③?? C? ⑤>③>①? D ④>③>②
参考答案:C
本题解析:略
本题难度:简单