微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知A、Y为常见金属单质,且Y是短周期元素,Z既可溶于盐酸,又可溶于氢氧化钠溶液。
据图回答问题:
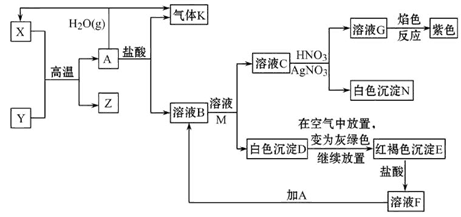
(1)Y在元素周期表中的位置_______________________。
(2)Z与氢氧化钠溶液反应的离子方程式为____________________________。
(3)B与M反应的化学方程式为______________________________________。
(4)A与水蒸气反应的化学方程式为__________________________________。
(5)检验溶液F中阳离子的方法是____________________________________。
(6)在沸水中加入F的饱和溶液的离子方程式为_______________________。
参考答案:(1)第三周期ⅢA族????????????? (2)
本题解析:由溶液G的焰色反应呈紫色知,溶液G中含K+;由溶液C与AgNO3溶液反应生成白色沉淀N知,白色沉淀N为AgCl,C中含Cl-,则G为KNO3,C为KCl;红褐色沉淀E为Fe(OH)3,则白色沉淀D为Fe(OH)2,F为FeCl3,M为KOH,B为FeCl2,A为Fe,K为H2,X为Fe3O4;由“Y是短周期元素,Z既可溶于盐酸,又可溶于氢氧化钠溶液”知,Y为Al,Z为Al2O3。(5)检验Fe3+的方法是:取少量待测液于试管中,滴加KSCN溶液,溶液呈红色
本题难度:一般
2、实验题 利用某炉渣 (只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
(只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
①用3.00mol/L的盐酸稀盐酸浸取炉渣,过滤.
②滤液先用H2O2氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3
③将第②步分离出沉淀的滤液通CO2调pH值后,保持温度在90~100℃进行“蒸发浓缩”,可以得到碱式氯化铝[Al2(OH)nCl6-n]
据以上信息回答下列问题:
(1)实验室配制3.00mol/L的盐酸100mL需要36.5%的浓盐酸(密度为1.2g/cm3)??? _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、?????????????。
(2)写出H2O2与滤液反应的化学方程式????????????????????
(3) “蒸发浓缩”需保持温度在90~100℃,可采用的加热方法是????????????????????
(4)为验证炉渣中含有Fe2O3,做如下实验:
a取适量炉渣于烧杯中,加足量????溶解、静置
b取上层清液少量于试管中,滴加???????,观察现象。选用提供的试剂,
提供的试剂:①稀硝酸 ②稀硫酸 ③氯水 ④KMnO4溶液 ⑤ KSCN溶液
步骤a、b中所加试剂分别为????????;
步骤b中反应的离子方程式:?????????????
参考答案: 本题解析:略
本题解析:略
本题难度:一般
3、选择题 由FeO、Fe2O3、Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21∶8,则这种混合物中FeO、Fe2O3、Fe3O4的物质的量之比可能为(??? )
①1∶1∶1?②1∶2∶1?③1∶2∶3?④1∶1∶3
A.①和②
B.②和③
C.③和④
D.①和④
参考答案:D
本题解析: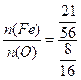 ?=3∶4。
?=3∶4。
可用代入法找出答案中铁与氧物质的量之比为3∶4 的即可。Fe3O4任意比,当FeO与Fe2O3满足物质的量之比为1∶1时即符合题意。
本题难度:简单
4、填空题 A、B、C、D为四种中学化学中常见的单质。常温时A为淡黄色固体,B也是固体且B可被磁化;C和D是双原子分子的气体,C呈黄绿色。E、F、G、H、I为五种化合物,E难溶于水,F为气体,且极易溶于水得无色酸性溶液;H溶于水后得黄色或棕黄色溶液。它们之间有如下反应的转化关系:
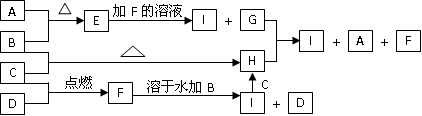
(1)四种物质的化学式:B________,C_______,E________,F_______;
(2)物质I溶液的颜色呈_______色;
(3)用实验方法鉴别H和I可用__________试剂,现象是_________________;
 (4)写出G+H??? I+A+F的离子方程式_______________________________。
(4)写出G+H??? I+A+F的离子方程式_______________________________。
参考答案:(1)B:Fe?? C:Cl2?? E:FeS?? F:HC
本题解析:
A为淡黄色固体,A为S; B也是固体且B可被磁化,?B为Fe; C呈黄绿色?C为Cl2;? D为H2;? E为FeS;? F为HCl; G为H2S; H为FeCl3 ;I为FeCl2
(1)B:Fe?? C:Cl2?? E:FeS?? F:HCl
(2)浅绿色
(3)KSCN????溶液显血红色
(4)2Fe3+ + H2S = 2Fe2+ + S + 2H+
本题难度:一般
5、选择题 金山铁路支线即上海轨交22号线运营采用动车组列车,最高时速可达160公里/小时。下列有关说法中正确的是
A.铁路勘探时常用太阳能电池提供能量,太阳能电池是原电池
B.铁轨焊接时常用到铝热反应,铝热反应中放出大量的热足以使铁熔化
C.铁元素在周期表中位于第四周期ⅡB族
D.工业上铁、铝的冶炼均采用热还原法
参考答案:B
本题解析:
试题分析:原电池是把化学能转化为电能的装置,太阳能电池是把太阳能转化为电能的装置,不是原电池,A不正确;铁元素在周期表中位于第四周期第Ⅷ族,选项C不正确;铝是活泼性金属,应该用电解法冶炼,D不正确,答案选B。
点评: 该题是基础性试题的考查,侧重对学生基础知识的检验和训练,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于调动学生的学习兴趣和学习积极性,难度不大。
本题难度:一般