��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
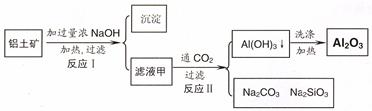
1������� ��14�֣�������(��Ҫ�ɷ�ΪAl2O3��SiO2��Fe2O3)����ȡ��������ԭ�ϡ���ȡ�������Ĺ����������£�
 ??
??
��1����Һ����Ҫ�ɷ��ǣ�д��ѧʽ��????????????������������������������
��2��д����Ӧ II �����ӷ���ʽ��??????????????????????????????????????????????????
��3����Ϸ�ӦII���ж�������������� ( H+) ����������ǿ������˳����????????������ĸ��ţ�
A��AlO2�D?????? B��OH�D??????? C��SiO32�D
��4��ȡ��Һ������������������ᣬ���ˣ����ö��Ե缫�������Һ���������������������ȫ���ݳ��������������г������ɣ���������ʧ��������ʧ��ԭ��������ӷ���ʽ��ʾΪ��???????????????????????????????????????????????????????????????????
��5��ȡ ��4�� ����Ժ����Һ 10.0 mL��������������Һ��ֻ�������ֵ����ʵ���Ũ�ȵļ������ʣ���������μ���0.100 mol? L��1������Һ��������50.0mL ������Һʱ�����ɵij���ǡ���ܽ⡣
�ټ���50.0mL ������Һ���������ӷ�Ӧ���Ⱥ�˳������Ϊ��????????????????????
���뻭�����ɳ��������ʵ����������������Ĺ�ϵͼ��
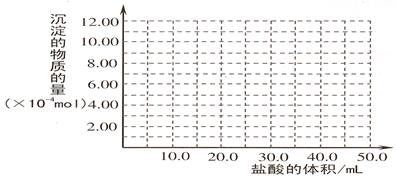
2��ʵ���� ��ͼ����ʾװ�õ�ʵ�����£��ȹر�K��ʹA�з�Ӧ���У����Ȳ�����C���ɹ۲쵽C���з���ҫ�۰⣬�������̣��ܱ��ϸ����е���ɫ���ʡ�ʵ����ɺ�C���й���ȫ�����������У��г�������ζ���������ɡ�
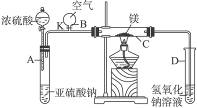
��1��C�е�MgӦ���ڲ���ֵ�Ƭ�϶�����ֱ�ӽӴ��ܱڣ�������Ϊ___________________
______________________________________________________________________________��
��2��ֹͣʵ��ʱ���ȴ�K����ֹͣ�μ�Ũ���ᲢϨ��ƾ��ƣ�������B��ʵ���е�������______________________________________________________________________________��
��3��C��ȫ����Ӧ������______________��______________��______________�����ѧʽ��
3�������� ��10�֣���þ�Ͻ����ѳ�Ϊ�ִ����졢������������ҵ����Ҫԭ�ϡ�����һ����þ�Ͻ����ⶨ����þ��������������λͬѧ�ֱ��ȡc����Ʒ��������˲�ͬ��ʵ�鷽����
�ף���þ�Ͻ� �����������������ml��������ɱ�״������
�����������������ml��������ɱ�״������
�ң���þ�Ͻ� ���ʣ����������a�ˣ�?
���ʣ����������a�ˣ�?
������þ�Ͻ� ��Һ
��Һ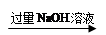 ��ó���������b�ˡ�
��ó���������b�ˡ�
��1��д���������йط�Ӧ�����ӷ���ʽ��?��������������������������������������
�÷����ܷ�ⶨ��þ������������������������ܡ����ܡ�����
��2���ҷ�����������Լ��������������ⶨ��þ����������Ϊ??????????��
��3����������ó���������Ϊb�ˣ��ӹ�����NaOH��Һ��ַ�Ӧ����??������һ�ַ��뷽������ϴ�ӡ���ɳ�������c=40��b=2.9������þ����������Ϊ��??�������δϴ�ӳ��������þ���������������������ƫ����ƫС������Ӱ�족����
4��ѡ���� ��5.1gMgAl�Ͻ��ܽ��ڹ�����500mL2mol/L�������У�Ȼ�����4mol/LNaOH��Һ����Ҫʹ���ɵij�����࣬��Ӧ���������NaOH��Һ�������
A��200mL
B��250 mL
C��425mL
D��560mL
5��ѡ���� �ۻ��������ع���Ӧѡ�õ������ǣ�???��
A��������
B��ʯӢ����
C������������
D��������