微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 火山爆发产生的气体中含有1%的羰基硫(化学式为COS,C===O就是羰基),已知羰基硫分子中所有原子最外层均满足8电子稳定结构,结合元素周期表知识,下列有关说法正确的是( )
A.羰基硫中O为-2价,C、S都是+1价
B.羰基硫分子中共含有3个原子核、16个电子
C.羰基硫分子结构中只含有共价键
D.羰基硫的电子式为?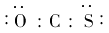
参考答案:C
本题解析:在分子中碳原子形成2个双键,电子式为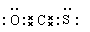 ,D不正确。其中双键都是偏离碳原子的,所以碳的化合价是+4价,氧和硫都是-2价,A不正确。羰基硫分子中共含有3个原子核、电子是6+8+16=30,B不正确。C、O、S都是非金属,形成的化学键是极性键,C正确。答案选C。
,D不正确。其中双键都是偏离碳原子的,所以碳的化合价是+4价,氧和硫都是-2价,A不正确。羰基硫分子中共含有3个原子核、电子是6+8+16=30,B不正确。C、O、S都是非金属,形成的化学键是极性键,C正确。答案选C。
本题难度:一般
2、选择题 下列反应盐酸作还原剂的是
A.CuO+2HCl=CuCl2+H2O
B.CaCO3+2HCl=CaCl2+CO2↑+H2O
C.2HCl+Zn=ZnCl2+H2↑
D.2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
参考答案:D
本题解析:分析:失电子化合价升高的反应物是还原剂,盐酸作还原剂说明反应前后盐酸中的元素失电子化合价升高,据此分析解答.
解答:A.该反应中,盐酸中的各元素化合价都不发生变化,所以盐酸不是还原剂,故A不选;
B.该反应中,盐酸中的各元素化合价都不发生变化,所以盐酸不是还原剂,故B不选;
C.该反应中,盐酸中的氢元素化合价降低,所以盐酸是氧化剂,故C不选;
D.该反应中,盐酸中的部分氯元素化合价升高部分不变,所以部分盐酸作还原剂,故D选;
故选D.
点评:本题考查了氧化还原反应,根据元素化合价变化来分析解答即可,难度不大.
本题难度:困难
3、选择题 25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是

A.2H+(aq) +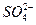 (aq)+
(aq)+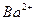 (aq)+2OH
(aq)+2OH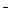 (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H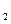 O(1);
O(1);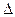 H=
H=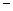 57.3 kJ/mol
57.3 kJ/mol

B.KOH(aq)+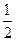 H
H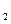 SO4(aq)=
SO4(aq)= 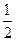 K
K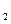 SO4(aq)+H
SO4(aq)+H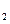 O(I);
O(I);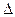 H=
H=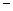 57.3kJ/mol
57.3kJ/mol

C.C8H18(I)+ 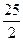 O
O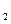 (g)=8CO
(g)=8CO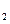 (g)+ 9H
(g)+ 9H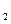 O;
O;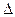 H=
H=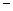 5518 kJ/mol
5518 kJ/mol

D.2C8H18(g)+25O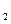 (g)=16CO
(g)=16CO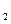 (g)+18H
(g)+18H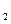 O(1);
O(1);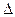 H=
H=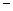 5518 kJ/mol
5518 kJ/mol


参考答案:B
本题解析:A项不符合中和热的定义;C项中生成物水为气态,D项中辛烷的物质的量不是1mol,所以ACD错误。
本题难度:一般
4、填空题 在下列物质中:①NaOH、②H2O2、③NH4Cl、④Na2O2、⑤C2H2、⑥SiC晶体?⑦Na2S⑧单晶硅。用序号回答下列问题:
⑴含有极性共价键的原子晶体是?????;
⑵只含有离子键的离子晶体是?????;
⑶既含有离子键又含有非极性共价键的离子晶体是?????;
⑷ 既含有离子键,又含有极性共价键和配位键的离子晶体是?????;
⑸含有极性共价键和非极性共价键的非极性分子是?????;
⑹含有极性共价键和非极性共价键的极性分子是?????。
参考答案:(各2分共12分)⑴ ⑥ , ⑵ ⑦ ,⑶ ④, ⑷ ③ ,
本题解析:
试题分析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。离子间通过离子键形成的晶体是离子晶体,分子间通过分子间作用力形成的晶体是分子晶体,原子间通过共价键形成的空间网状结构的晶体是原子晶体,由金属阳离子和自由电子构成的晶体是金属晶体,据此可知:
⑴含有极性共价键的原子晶体是碳化硅,答案选⑥;
⑵只含有离子键的离子晶体是硫化钠,答案选⑦;
⑶既含有离子键又含有非极性共价键的离子晶体是过氧化钠,答案选④;
⑷ 既含有离子键,又含有极性共价键和配位
本题难度:一般
5、选择题 下列叙述正确的是( )
A.化合物中一定含有σ键,可能含π键
B.由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子里
D.不同元素组成的多原子分子里的化学键一定都是极性键
参考答案:B
本题解析:A不正确,例如离子化合物氯化钠中没有共价键。B正确,例如铵盐等。C不正确,例如双氧水中含有非极性键。D不正确,例如醋酸中含有非极性键。答案选B。
本题难度:一般