微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能正确表示下列反应的离子方程式为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+===Fe2++H2S↑
B.含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3―+Ba2++OH-===BaCO3↓+H2O
C.少量CO2通入硅酸钠溶液中:SiO32―+2CO2+2H2O===H2SiO3↓+2HCO3―
D.硫化钠水溶液呈碱性:S2-+2H2O H2S+2OH-
H2S+2OH-
参考答案:B
本题解析:
试题分析:A、硫化亚铁溶于稀硝酸中时,因硝酸具有强氧化性,可以将亚铁离子氧化为三价,也会将硫化氢氧化,所以产物中不会生成Fe2+和H2S,故A错误。
B、含等物质的量的KHCO3和Ba(OH)2溶液混合,钡离子和碳酸氢根按物质的量之比1:1反应,即HCO3―+Ba2++OH-=BaCO3↓+H2O,故B正确。
C、少量CO2通入硅酸钠溶液中:SiO32―+CO2+H2O===H2SiO3↓+CO32-,故C错误。
D、硫化钠中的硫离子是多元弱酸根离子,分步水解,以第一步为主,为:
本题难度:一般
2、填空题 离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有???????(填序号)。
①单质;②氧化物;③电解质;④盐;⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。
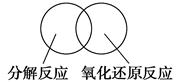

(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
①所有的离子方程式均可以表示一类反应
| ?
|
②酸碱中和反应均可表示为H++OH-=H2O
| ?
|
③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号
| ?
?
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO42-=BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
①?????????????????????????????????????????????????????????????;
②?????????????????????????????????????????????????????????????;
③????????????????????????????????????????????????????????????。
参考答案:(1)③⑤
(2) 本题解析:离子反应中一定有离子参与反应或有离子生成,因此一定有电解质(化合物)参与反应或生成。置换反应一定是氧化还原反应,二者有一部分可用离子方程式表示,如Zn+Cu2+=Cu+Zn2+,有的则只能用化学方程式表示,如CuO+H2 本题解析:离子反应中一定有离子参与反应或有离子生成,因此一定有电解质(化合物)参与反应或生成。置换反应一定是氧化还原反应,二者有一部分可用离子方程式表示,如Zn+Cu2+=Cu+Zn2+,有的则只能用化学方程式表示,如CuO+H2 Cu+H2O。 Cu+H2O。
本题难度:一般
3、选择题 下列离子方程式正确的是
A.用惰性电极电解熔融氯化钠:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH-
B.稀硝酸中加入少量铁粉:2Fe+6H+= 2Fe3++3H2↑
C.用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2=NO3-+NO↑+H2O
D.0.01mol・L-1NH4Al(SO4)2溶液与0.02mol・L-1Ba(OH)2溶液等体积混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3・H2O
参考答案:D
本题解析:
试题分析:A项:违法客观事实,熔融态不会有水,故错;B项:违法客观事实,硝酸有很强的氧化性,与金属反应不生成氢气,故错;C项:电荷不守恒,故错。故选D。
点评:离子方程式正误判断要注意:看原则:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。
本题难度:简单
4、填空题 (10分)在四个脱落标签的试剂瓶中,分别盛有盐酸、BaCl2溶液、Na2CO3溶液、AgNO3溶液,为了鉴别各瓶试剂将它们分别编号为A、B、C、D两两混合,其实验现象为:
A+B→无色气体????? B+C→白色沉淀???? A+D→白色沉淀?? A+C→无明显现象
(1)由此推断各试剂瓶中所盛试剂为(填化学式)
A:?????????B:?????????C:?????????D:??????????
(2)写出下列反应的离子方程式
①A+B:??????????????????②B+C:?????????????? ???????③A+D:?????????????????? ???????③A+D:??????????????????
参考答案:(1)A:?? HCl? B:??? Na2CO3??? C
本题解析:略
本题难度:简单
5、选择题 下列离子方程式中,正确的是(????)
A.水玻璃中通入足量的CO2: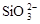 +2CO2+2H2O==H2SiO3↓+2CO +2CO2+2H2O==H2SiO3↓+2CO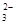
B.氯化亚铁溶液中通入足量的Cl2:2Fe2++Cl2==2Fe3++2Cl-
C.NaHCO3溶液中加入足量NaHSO4溶液: 2H++CO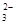 ==CO2↑+H2O ==CO2↑+H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3―+ Ba2+ + 2OH―= BaCO3↓ +2H2O + CO32―
参考答案:B
本题解析:
试题分析:A不正确,CO2过量生成的是碳酸氢钠;C不正确,应该是H++HCO3-=H2O+CO2↑;D不正确,氢氧化钡过量,生成物是碳酸钡、氢氧化钠和水,答案选B。
点评:判断离子方程式正确与否的方法一般是:(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式。
本题难度:困难
|