微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以下电离方程式书写正确的是
A. H2S 2H++S2-
2H++S2-
B.CaCO3=Ca2++CO32-
C. NaHCO3 Na++HCO3-
Na++HCO3-
D.NaHS = Na++H++S2-
参考答案:B
本题解析:略
本题难度:简单
2、选择题 下列事实一定能说明HNO2为弱电解质的句数是
①常温时NaNO2溶液的pH大于7;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2与NaCl不能反应;
④常温下0.1 mol・L-1的HNO2溶液pH=2;
⑤1 L pH=1的HNO2溶液加水稀释至100 L后溶液的pH=2.2;
⑥1 L pH=1的HNO2溶液和1 L pH=1的盐酸分别与足量的NaOH溶液完全反应,最终HNO2消耗的NaOH多;
⑦HNO2溶液中加入一定量的NaNO2晶体,溶液中c(OH-)增大;
⑧HNO2溶液中加水稀释,溶液中c(OH-)增大。
A.4句
B.5句
C.6句
D.7句
参考答案:B
本题解析:
试题分析:①常温下NaNO2溶液,根据盐类水解的规律,无弱不水解,有弱才水解,越弱越水解,谁强显谁性,如果NaNO2是强酸强碱盐,PH=7,而题干中PH>7,说明NaNO2为强碱弱酸盐,故①正确;②溶液的导电性与离子的浓度有关,弱电解质的浓度大时导电实验中灯泡也很亮,没有对比实验,无法说明HNO2是弱电解质,故错误;③HNO2与NaCl不能反应,无论亚硝酸是强酸还是弱酸,它们间都不反应,故③错误;④常温下,0.1mol/L的HNO2溶液的pH为2,说明亚硝酸只有部分电离,所以能说明是弱酸,故正确;⑤1 L pH=1的HNO2溶液加水稀释至100 L后溶液的pH=2.2,pH<4,说明 亚硝酸中存在电离平衡,所以能说明是弱酸,故正确;
考点:强电解质和弱电解质的概念
本题难度:一般
3、简答题 25℃时,电离平衡常数:
| 化学式 | CH3COOH | H2CO3 | HClO
电离平衡常数
1.8×10-5
K1=4.3×10-7
K2=5.6×10-11
3.0×10-8
回答下列问题:
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa? d.NaHCO3;pH由大到小的顺序是:______;(填编号)
(2)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是:______;
A.c(H+)???B.c(H+)/c(CH3COOH)?C.c(H+)?c(OH-)??D.c(OH-)/c(H+)
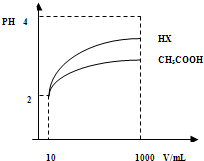
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图.则HX的电离平衡常数______(填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是______,稀释后,HX溶液中水电离出来的c(H+)______醋酸溶液水电离出来c(H+)(填“大于”、“等于”或“小于”)理由是:______;
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO-)-c(Na+)=______.(填准确数值).
参考答案:(1)由电离平衡常数判断酸性的强弱,酸性越强,其对应盐的水解
本题解析:
本题难度:一般
4、选择题 对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.使温度都升高20℃后,两溶液的pH均不变
C.加水稀释2倍后,醋酸溶液的pH变化程度大
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
参考答案:A
本题解析:
本题难度:一般
5、选择题 25℃ 时,水的离子积为Kw,该温度下将 a mol ・L-1一元酸 HA 与b mol・L-1一元强碱BOH 等体积混合,若恰好完全反应,下列结论中不正确的是
A. 混合液中:c(H+ ) ≤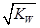 ???????B. 混合液中:c(HA)+c(A-)=a mol・L-1?? ???????B. 混合液中:c(HA)+c(A-)=a mol・L-1??
C.? a = b??????????????????????D. 混合液中:c(H+)+c(B+)= c(OH-)+c(A-)
参考答案:B
本题解析:
试题分析: HA 与BOH 等体积混合,恰好完全反应:HA+BOH==BA+H2O,酸和碱的物质的量相同,故C正确;根据电荷守恒,D正确;若HA为强酸,反应后的盐溶液为中性,c(H+)=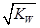 ;若HA为若酸,反应后的盐溶液为碱性,c(H+)< ;若HA为若酸,反应后的盐溶液为碱性,c(H+)< 本题难度:一般 本题难度:一般
|