微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么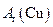 ?(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
?(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量 m(H20),由此计算
m(H20),由此计算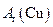 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):

请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)=" a" g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大 的是_______________ (填序号);
的是_______________ (填序号);
1Cu0未完全起反应?????????② CuO不 干燥
干燥
3Cu0中混有不反应的杂质???④碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________ _____和_______________达到实验目的。
_____和_______________达到实验目的。
2、实验题 某研究小组进行与NH3有关的系列实验。
(1)从下图中挑选所需仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。
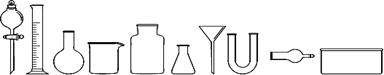
(2)将NH3通入溴水中,有N2生成,反应的化学方程式为????????????????????。
3、实验题 (12分)(1)某化学小组的同学在学习了NaHCO3和Na2CO3的有关知识后,进行如下实验:在两支试管中分别加入3mL4 mol・L-1稀盐酸,将两个各装有0.3g NaHCO3或 Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:

①试管中(填产生沉淀或气体及反应速率等相关现象)___________??????????????_。
②盛______________的试管中气球变得更大,大小气球体积之比约为(填简单整数比)____________;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3
的试管温度有升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。类似如中和热,甲同学写出了下列热化学方程式:
HCO3-(aq)+H+(aq)=H2O(l)+CO2(g);?△H>0
CO32-(aq)+2H+(aq)=H2O(l)+CO2(g);?△H<0
甲下结论的方法是否正确____________(填“正确”或“不正确”)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
序号
| 试剂1
| 试剂2
| 混合前温度
| 混合后最高或最低温度
|
①
| 35mL水
| 2.5g NaHCO3固体
| 20℃
| 18.5℃
|
②
| 35mL水
| 3.2g Na2CO3固体
| 20℃
| 24.3℃
|
③
| 35mL
稀盐酸
| 含2.5g NaHCO3的饱和溶液32.5mL
| 20℃
| 19℃
|
④
| ?35mL
稀盐酸
| 含3.2g Na2CO3的饱和溶液23.1 mL+10ml水
| 20℃
| 24.2℃
|
⑤
| ?35mL
稀盐酸
| 2.5gNaHCO3固体
| 20℃
| 16.2℃
|
⑥
| ?35mL
稀盐酸
| 3.2g Na2CO3固体
| 20℃
| 25.1℃
请你帮助填写相关内容:
①该研究报告的题目是《_____________________________________》;
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为_________和__________;通过上述实验可得出五条结论(用“吸热”或“放热”填写):
a:NaHCO3的溶解是_______过程;
b:Na2CO3的溶解是_______过程;
c:NaHCO3的饱和溶液和盐酸的反应是____________反应;
d:Na2CO3的饱和溶液和盐酸的反应是____________反应;
e:NaHCO3固体与稀盐酸反应的反应热是______(填a、b、c、d中的字母)的热效应之和。
4、实验题 (12分)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
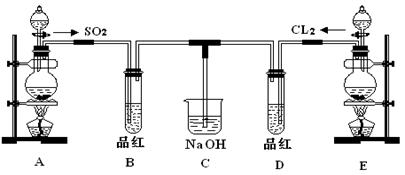
(1)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:_________________ _______________,D:____________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:
B:________________________________,D:____________________________。
(2)实验中NaOH溶液的作用是:______________________________________ 。
写出Cl2通入NaOH溶液中的化学方程式_______________________________。
5、实验题 Na2CO3是很重要的化学物质,某学生拟在实验室中制备Na2CO3。下面是他的制备实验过程:
将50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:
(Ⅰ)用25mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;(Ⅱ)小心煮沸溶液1~2分钟;(Ⅲ)在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
请回答下列问题:
(1).在(Ⅰ)中,刚通入CO2时发生的反应是??????????????????????????????????;而后又发生反应????????????????????????????????????。(请写出化学方程式)
(Ⅱ)中煮沸溶液的目的是?????????????????????????????????????????????。
(Ⅲ)中混合另一半NaOH溶液后发生的反应是??????????????????(请写出离子方程式)
评价该同学能否制得较纯净的Na2CO3?????????????????。(填“能”或“不能”)
(2).按该同学的设计,第(Ⅰ)步实验装置如下:
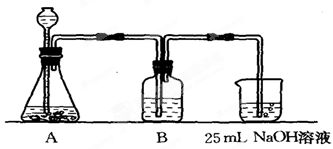
①装置A使用的试剂是??????????????(固体)和?????????????溶液;
②装置B使用的试剂最好是???????????(选择:水、饱和NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液),作用是????????????????????????;如果不用B装置,最终得到的Na2CO3溶液中可能存在的杂质有???????????????????????????。
|