��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����������ʯ��ˮ����250 mL̼������Һ�У����ˡ������õ�10 g������
�Ŵ�̼������Һ�����ʵ���Ũ��Ϊ________________ __________��
����ȡ����10 g�����������м��������ϡ�����ַ�Ӧ�������ղ����������ڱ�״���µ����ԼΪ ����Ҫһ������ȫ�ռ���Щ���壬����Ϊ�ܷ���ʵ��������ͨ�ļ���ƿ�����ռ��𣿣���ش��ܡ����ܡ��� �������ܣ���ô����Ϊ���� ���ռ���Щ���塣
�ο��𰸣�����0.4 mol��L��1
���������
���������(1)�⣺Na2CO3+Ca(OH)2=CaCO3 ��+2NaOH
1 1
n(Na2CO3) 10g/100g.mol-1
n(Na2CO3)=0.1mol
c (Na2CO3)=0.1mol/0.25L=0.4mol/L
(2)�⣺ CaCO3+2HCl=CaCl2+H2O+CO2��
1 mol 22.4L
0.1mol V(CO2)
V(CO2)=2.24L
���㣺���ʵ����ڻ�ѧ����ʽ������Ӧ�á�������̼������ռ���
������������Ҫ����ѧ���������ʵ����ڻ�ѧ����ʽ������Ӧ�õ�������ͬʱ�����˶�����̼������ȡ�����֪ʶ��������ѧ�����������˼ά��ȣ�ǿ����ѧ������ ֪ʶ��������
�����Ѷȣ�һ��
2��ѡ���� ���¡���ѹ�������������壺H2��D2��������������ȷ����
���ܶ�֮��Ϊl�U2??????????????????��������֮��Ϊ2�U1????�����֮��Ϊ2�U1
A���٢ڢ�
B���ڢ�
C���٢�
D���٢�
�ο��𰸣�D
������������¡���ѹ�������������壺H2��D2�����ʵ���֮��Ϊ2:1�����֮��Ϊ2�U1��
�ܶ�֮�ȵ���Ħ������֮��Ϊl�U2��������֮��Ϊ2��2�U1��4= 1:1
�����Ѷȣ�һ��
3�������� 3.84 g Fe��Fe2O3�Ļ�������ڹ��������У�����0.03 mol H2����Ӧ�����Һ�м���KSCN��Һ���飬��Һ���Ժ�ɫ����ԭ�������Fe2O3��������
�ο��𰸣�1.6g
���������
���������������Һ�м�KSCN��Һ���Ժ�ɫ˵�����в���Fe3+������ΪFeCl2���ܷ�Ӧ�ɱ�ʾΪFe+Fe2O3+HCl��FeCl2+H2��+H2O������������Ϊx���ɵ�ʧ������ȵã�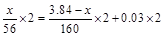 ����ã�x=2.24g��
����ã�x=2.24g��
�������й�������ԭ��Ӧ�ļ������õ�ʧ������ȼ���ɿ��ٽ��⡣
�����Ѷȣ�һ��
4��ѡ���� MgCl2��Һ��Na2SO4��Һ��Ϻ�c(Mg2+)=c(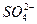 )��������˵������ȷ���ǣ�???��
)��������˵������ȷ���ǣ�???��
A�����Һ��c(Cl-)=c(Na+)
B�����Һ��c(Cl-)=2c(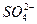 )
)
C�����ǰ����Һ������
D�����ǰ����Һ��MgCl2��Na2SO4���ʵ������
�ο��𰸣�C
���������������Һ����غ㣬c(Na+)+2��c(Mg2+)=c(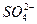 )��2+c(Cl-)������Ϊ?c(Mg2+)=c(
)��2+c(Cl-)������Ϊ?c(Mg2+)=c(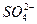 )������
)������
�����Ѷȣ���
5������� ����18.4mol?L-1��ŨH2SO4������250mL��0.300mol?L-1��ϡH2SO4���ɹ�ѡ��������У�
��ҩ�ע���Ͳ��������ƽ�ܲ���������ƿ?��ͷ�ιܢ�����ƿ���ձ���
��ش��������⣺
��1�����������У�������ϡH2SO4ʱ�ò�������______������ţ���
��2�������㣬��ŨH2SO4�����Ϊ______�����Т�5mL��10mL��20mL���ֹ����Ͳ����ѡ�õ���Ͳ��______������ţ���
�ο��𰸣���1�����Ʋ�������ȡ��ϡ�͡���ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�
���������
�����Ѷȣ�һ��