微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现有常温下的0.1 mol/l纯碱溶液。
(1)该溶液呈碱性是因为存在水解平衡,相关离子方程式是:________________。为证明存在上述平衡,进行如下实验:在0.1 mol・l-1纯碱溶液中滴加酚酞,溶液显红色,再往溶液中滴加 (填化学式)溶液,红色逐渐退为无色,说明上述观点成立。
(2)同学甲查阅资料得知0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。请设计实验加以证明(写出实验方案及预期观察到的现象)。答: 。
(3)同学乙就该溶液中粒子浓度关系写出五个关系式,其中不正确的是 。
A.c(Na+)>2c(CO32―)
B.c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)
C.c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)
D.c(CO32―)+c(HCO3―)="0.1" mol・L-1
E.c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+c(CO32―)
(4)室温下pH均为a的Na2CO3和NaOH溶液中,水电离产生的c(OH―)之比= 。
参考答案:(1)CO32- + H2O 本题解析:
本题解析:
试题分析:(1) 纯碱碳酸钠是强碱弱酸盐。在溶液中存在的水解平衡主要是CO32- + H2O HCO3- + OH-,还有HCO3- + H2O
HCO3- + OH-,还有HCO3- + H2O H2CO3-+ OH-。由于消耗了水电离产生的H+,所以最终使溶液中的c(OH-)>c(H+)。因此溶液显碱性。再往溶液中滴加与CO32-形成沉淀的物质如BaCl2或CaCl2,此时会放出沉淀反应,消耗了CO32-,c(CO32-)减小,尽管水解程度增大,但是单位体积中的OH-的物质的量减少,所以溶液的碱性减弱,红色逐渐退为无色。(2)在Na2CO3溶液中主要存在水解平衡CO32- + H2O
H2CO3-+ OH-。由于消耗了水电离产生的H+,所以最终使溶液中的c(OH-)>c(H+)。因此溶液显碱性。再往溶液中滴加与CO32-形成沉淀的物质如BaCl2或CaCl2,此时会放出沉淀反应,消耗了CO32-,c(CO32-)减小,尽管水解程度增大,但是单位体积中的OH-的物质的量减少,所以溶液的碱性减弱,红色逐渐退为无色。(2)在Na2CO3溶液中主要存在水解平衡CO32- + H2O HCO3- + OH-。c(CO32-)(始)=" 0.1" mol/L,若其水解程度等于10%,根据水解方程式可知:c(OH-)=0.01mol/L.c(H+)=10-12mol/L.pH=12.水解程度越大,水解产生的c(OH-)就越高,溶液的pH就越大。若水解程度小于10%,则c(H+)>10-12mol/L.pH<12.因此,测0.1 mol・L-1Na2CO3溶液pH,若pH≤12就证明0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。(3)A根据物料守恒可得c(Na+)=2c(CO32―)+2 c(HCO3―)+2c(H2CO3).所以c(Na+)>2c(CO32―) 。正确。B.在Na2CO3中存在水解平衡:CO32- + H2O
HCO3- + OH-。c(CO32-)(始)=" 0.1" mol/L,若其水解程度等于10%,根据水解方程式可知:c(OH-)=0.01mol/L.c(H+)=10-12mol/L.pH=12.水解程度越大,水解产生的c(OH-)就越高,溶液的pH就越大。若水解程度小于10%,则c(H+)>10-12mol/L.pH<12.因此,测0.1 mol・L-1Na2CO3溶液pH,若pH≤12就证明0.1 mol/LNa2CO3中,发生水解的CO32―不超过其总量的10%。(3)A根据物料守恒可得c(Na+)=2c(CO32―)+2 c(HCO3―)+2c(H2CO3).所以c(Na+)>2c(CO32―) 。正确。B.在Na2CO3中存在水解平衡:CO32- + H2O HCO3- + OH-, HCO3- + H2O
HCO3- + OH-, HCO3- + H2O H2CO3-+ OH-。主要是第一步水解,所以c(HCO3―)> c(H2CO3);但是盐水解的程度是很微弱的,盐的电离作用大于水解作用,所以c(CO32―)> >c(HCO3―)。由于两步水解都产生OH-,HCO3―第一步水解产生,而在第二步水解中由消耗。所以c(OH-)>c(HCO3―)。因此在溶液中离子间的关系为: c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)。正确。C.溶液显碱性。根据质子守恒可得:c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)。正确。D.根据物料守恒可得c(CO32―)+c(HCO3―)+ c(H2CO3)="0.1" mol/L.错误。E.根据电荷守恒可得c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+2c(CO32―).错误。(4)室温下pH均为a的Na2CO3溶液,c(H+)=10-a, c(OH-)(水)=10-14÷10-a =10a-14mol/L.对于pH=a的NaOH溶液c(H+)(水)= c(OH-)(水)=10-amol/L.所以水电离产生的c(OH―)之比=10a-14:10-a=10(2a-14)。
H2CO3-+ OH-。主要是第一步水解,所以c(HCO3―)> c(H2CO3);但是盐水解的程度是很微弱的,盐的电离作用大于水解作用,所以c(CO32―)> >c(HCO3―)。由于两步水解都产生OH-,HCO3―第一步水解产生,而在第二步水解中由消耗。所以c(OH-)>c(HCO3―)。因此在溶液中离子间的关系为: c(CO32―)>c(OH-)>c(HCO3―)>c(H2CO3)。正确。C.溶液显碱性。根据质子守恒可得:c(OH-)=c(H+)+c(HCO3―)+2c(H2CO3)。正确。D.根据物料守恒可得c(CO32―)+c(HCO3―)+ c(H2CO3)="0.1" mol/L.错误。E.根据电荷守恒可得c(H+)+ c(Na+)= c(OH-)+c(HCO3―)+2c(CO32―).错误。(4)室温下pH均为a的Na2CO3溶液,c(H+)=10-a, c(OH-)(水)=10-14÷10-a =10a-14mol/L.对于pH=a的NaOH溶液c(H+)(水)= c(OH-)(水)=10-amol/L.所以水电离产生的c(OH―)之比=10a-14:10-a=10(2a-14)。
考点:考查盐的水解平衡、盐水解程度的测定、离子浓度的大小比较、相同pH的碱与盐的水的电离的知识。
本题难度:一般
2、选择题 已知水的电离方程式:H2O H++OH-,下列叙述正确的是 [???? ]
H++OH-,下列叙述正确的是 [???? ]
A.升高温度,Kw增大,pH不变
B.向水中加入少量硫酸,c(H+)增大,KW不变
C.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低
D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低
参考答案:B
本题解析:
本题难度:一般
3、选择题 能使水的电离平衡右移,且水溶液显酸性的微粒是( ? )
A.Al3+
B.OH-
C.H+
D.HCO3-
参考答案:A
本题解析:
本题难度:简单
4、填空题 (8分)已知水在25 ℃和95 ℃时,其电离平衡曲线如图所示。
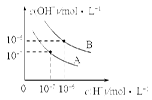
(1)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是________。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1________α2(填“大于”、“小于”、“等于”或“无法确定”),若二者恰好反应所得溶液的pH<7,原因是__________________。(用离子方程式表示)
(4)在曲线B所对应的温度下,将0.02 mol/L的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=________。
参考答案:(8分)(1) 10:1(2分);(2)a+b=14 (2分
本题解析:
试题分析:(1)25℃时, pH=9的NaOH溶液,c(OH-)=10-5mol/L;pH=4的H2SO4溶液混合,c(H+)=10-4mol/L;若所得混合溶液的pH=7,n(OH-)=n(H+)。则c(OH-)?V(NaOH)= c(H+)?V(H2SO4)。故NaOH溶液与H2SO4溶液的体积比为V(NaOH):V(H2SO4)= c(H+):c(OH-)=10:1;(2)95℃时,水的离子积常数是Kw=10-13.若100体积pH=a的某强酸溶液中n(H+)=100×10-amol=10(2-a)mol, 1体积pH=b的某强碱溶液n(OH-)=10-12÷10-b=10(b-12)mol。混合后溶液呈中性,10(2-a)mol=10(b-12)mol。2-a=b-12.所以a+b=14。(3)曲线A所对应的温度是室温。在室温下,pH=2的HCl溶液,c(H+)(水)=10-12mol/L;pH=11的某BOH溶液中,c(H+)(水)=10-11mol/L;水电离产生的H+的浓度越大,水的电离程度就越大。若水的电离程度分别用α1、α2表示,则α1<α2。若二者恰好反应所得溶液的pH<7,说明该盐是强碱弱酸盐,弱碱阴离子B-发生水解反应消耗水电离产生的H+,最终使溶液中c(H+)>c(OH-),水解的离子方程式是:B- + H2O BOH + H+;(4)曲线B所对应的温度是95 ℃,该温度下水的离子积常数是Kw=10-12,在曲线B所对应的温度下,将0.02 mol/L的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,则反应后溶液中c(OH-)=0.02mol÷2L=0.01mol/L。由于该温度下水的离子积常数是Kw=10-12,所以c(H+)=10-10,所得混合液的pH=10。
BOH + H+;(4)曲线B所对应的温度是95 ℃,该温度下水的离子积常数是Kw=10-12,在曲线B所对应的温度下,将0.02 mol/L的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,则反应后溶液中c(OH-)=0.02mol÷2L=0.01mol/L。由于该温度下水的离子积常数是Kw=10-12,所以c(H+)=10-10,所得混合液的pH=10。
考点:考查酸碱中和反应时溶液的体积比、盐的水解、溶液的pH的计算的知识。
本题难度:一般
5、选择题 下列溶液一定呈中性的是( )
A.PH=7的溶液
B.0.1mol/L的Na2CO3溶液
C.c(H+)=1×10-7 mol/L
D.c(H+)=C(OH―)
参考答案:D
本题解析:
试题解析:PH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故A错误.0.1mol/L的Na2CO3溶液中,碳酸根离子水解,溶液呈碱性,故B错误;(H+)=10-7mol?L-1的溶液,溶液的PH=7,如A所分析,溶液不一定成中性,故C错误;溶液中当C(H+)=C(OH-)时,溶液一定呈中性,故D正确。
考点:溶液酸碱性的判断
本题难度:一般