微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 向30.0mL硫酸铜溶液中加入过量铝粉,待充分反应后,再向其中加入2.00mol/L烧碱溶液,至沉淀不再减少,消耗烧碱溶液210mL,且收集到气体0.672L(标准状况).据此计算:
(1)加入铝粉的质量.
(2)原硫酸铜溶液的物质的量浓度.
参考答案:发生反应的离子方程式为? 3Cu2++2Al=3Cu+2Al
本题解析:
本题难度:一般
2、选择题 若用NA表示阿伏加德罗常数的值,则下列说法错误的是
A.常温常压下22.4 LH2含2NA个电子
B.NA个O2和NA个H2的质量比为16:1
C.1molH2O总共含有3NA个原子
D.71g Cl2中共有17NA个质子
参考答案:AD
本题解析:
试题分析:A不正确,常温常压下,22.4L氢气的物质的量不是1mol;NA个O2和NA个H2的物质的量都是1mol,质量比为16:1,B正确;水是由2个氢原子和1个氧原子构成的,所以1molH2O总共含有3NA个原子,C正确;氯气分子中质子数是2×17=34个,71g氯气是1mol,含有34NA个质子,D不正确,答案选AD。
点评:阿伏加德罗常数是历年高考的“热点”问题,为高考必考题目,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知
本题难度:一般
3、填空题 (2分)27.2g某二价金属的氯化物ACl2中含有0.4m ol Cl-离子,ACl2的摩尔质量是 ,A的相对原子质量是 。
ol Cl-离子,ACl2的摩尔质量是 ,A的相对原子质量是 。
参考答案:136g/mol
本题解析:略
本题难度:一般
4、填空题 标准状况下,有氧气和氯气组成的混合气体共500mL。通入氢气,一定条件下使它们恰好完全反应,然后加水得到250mL盐酸溶液。从中取出25mL,用25mL 0.08mol・L-1 NaOH溶液恰好中和。则
(1)盐酸溶液的物质的量浓度?????????????mol・L-1。
(2)氢气的体积为????????????????mL。
参考答案:(1) 0.08?? (2)776
本题解析:
试题分析:(1)氢氧化钠的物质的量是0.025L×0.08mol/L=0.002mol,则根据反应的化学方程式HCl+NaOH=NaCl+H2O可知,参加反应的氯化氢的物质的量也是0.025mol,则盐酸的浓度是0.002mol÷0.025L=0.08mol/L。
(2)根据(1)可知,盐酸中氯化氢的物质的量是0.02mol,则根据氯原子守恒可知,氯气和与氯气反应的氢气的物质的量分别都是0.01mol,在标准状况下的体积都是224ml,所以原混合气中氧气的体积是500ml-224ml=276
本题难度:一般
5、选择题 在体积为VmL、密度为dg・cm-3的溶液中,溶有式量为M的溶质mg,其物质的量浓度为cmol・L-1,质量分数为w%,则下列表示式中正确的是
A.c=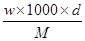
B.m=Vd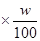
C.w%=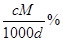
D.c=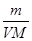
参考答案:B
本题解析:根据 ?可知,A、C不正确。D中应该是
?可知,A、C不正确。D中应该是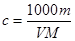 ,所以正确的答案选B。
,所以正确的答案选B。
本题难度:一般