微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 2 mol NaHCO3和1mol Na2O2固体在密闭容器中加热,使其充分反应,则最后容器中剩余的固体是??????? (???? )
A.只有Na2CO3
B.一定为Na2CO3和NaOH
C.可能有Na2O2
D.可能有NaOH
参考答案:A
本题解析:略
本题难度:简单
2、选择题 将0.2 mol????? Na投入到足量水中得a g溶液,将0.2 mol Mg投入到足量盐酸中得到b g溶液,则反应后两溶液质量关系为(???)
A.a="b"
B.a>b
C.a<b
D.无法判断
参考答案:A
本题解析:2Na―H2差量为4.6 g-0.2 g="4.4" g,Mg―H2差量为4.8 g-0.4 g="4.4" g。
本题难度:简单
3、实验题 某兴趣小组为测定某工业纯碱(假设仅含NaHCO3杂质)中Na2CO3的质量分数,设计了下列四种实验方案:
方案一:纯碱样品 测定剩余固体质量
测定剩余固体质量
(1)称取mg样品放入坩埚中充分加热。坩埚中发生反应的化学方程式为:?????????????????????????????????????????????
(2)将坩埚置于干燥器中冷却后称量。实验时需要重复“加热、冷却、称量”操作多次,其目的是:?????????????????????????????????????????????????。
方案二:称取mg样品配成250mL溶液,从中取25mL溶液先用酚酞作指示剂用0.1mol/LHCl溶液滴定至终点,消耗0.1mol/LHCl溶液V1mL,继续用甲基橙作指示剂滴定至终点,消耗0.1mol/LHCl溶液V2mL。则该样品中碳酸钠的质量分数为:???????????????????。
方案三:纯碱样品溶液 测定沉淀质量
测定沉淀质量
(1)称取m1g样品,置于小烧杯中,加水溶解后滴加足量氯化钙溶液。将反应混和物过滤后的下一步操作是:????????????????????????,沉淀经干燥后称量为m2g。
(2)如果用氢氧化钙溶液代替氯化钙溶液作沉淀剂,在其他操作正确的情况下,_______测定样品中的Na2CO3的质量分数。(填“能”或“不能”)
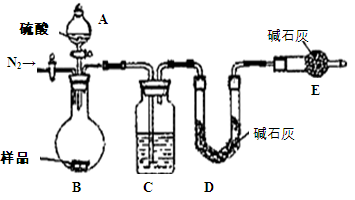
方案四:纯碱样品 测定生成二氧化碳的质量
测定生成二氧化碳的质量
(1)本实验采用如图装置,C中盛放的物质是????????????。
(2)反应前后都要通入N2,反应后通入N2的目的是:????????????????????????????????
参考答案:方案一:(1)2NaHCO3=Na2CO3+CO2↑+H2O
本题解析:
试题分析:方案一:该方案原理为:在加热条件下Na2CO3能够稳定存在,而NaHCO3易发生分解反应,从而根据残留的固体的量推算出样品中碳酸钠的质量分数;(1)坩埚中发生反应的化学方程式为:2NaHCO3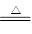 Na2CO3 + CO2↑+ H2O;(2)该方案根据加热后残渣的质量来求解,要加热至恒重,以保证Na
Na2CO3 + CO2↑+ H2O;(2)该方案根据加热后残渣的质量来求解,要加热至恒重,以保证Na
本题难度:困难
4、选择题 将一小块钠放在石棉网上加热,下列组合正确的是(??? )
①燃烧,黄色火星四射②金属熔化③燃烧火焰为黄色④燃烧生成白色固体
⑤燃烧生成淡黄色固体
A.②①
B.②①③
C.②③⑤
D.②③④
参考答案:C
本题解析:此题考查对Na燃烧这一化学实验的观察。Na在空气中燃烧时先熔成小球,燃烧时火焰为黄色但无火星,生成淡黄色固体,因此②③⑤正确,①④错误。
本题难度:简单
5、选择题 可以用来鉴别Na2CO3溶液和NaHCO3溶液最好的是
A.加CaCl2溶液
B.加热
C.加稀盐酸
D.加澄清的石灰水
参考答案:A
本题解析:鉴别效果应从操作的简易程度及现象是否明显来判定
加热操作较麻烦,排除;两溶液均可与澄清石灰水生成白色沉淀,排除;
两者均可与盐酸产生气体,排除,故答案为A:前者可产生白色沉淀,而后者无现象
本题难度:一般