微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (7分)现有22g Mg、Al、Zn、Fe多种活泼金属粉末的混合物与200mL含有一定质量的20%硫酸溶液恰好完全反应,得到无水盐70g,求(要求写出计算过程)
(1)硫酸溶液的质量?
(2)生成的气体体积(标准状况)?
(3)硫酸物质的量浓度?
参考答案:(1)m(SO42-)=m(无水盐)-m(金属)=70-22
本题解析:试题分析:金属与硫酸恰好反应生成硫酸盐与氢气,根据质量守恒可知m(SO42-)=80g-22g=48g,则n(H2SO4)=n(SO42-)=0.5mol,根据关系式H2SO4~H2↑计算氢气的体积;再根据c=n/v计算硫酸的物质的量浓度。
本题难度:一般
2、选择题 在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为[???? ]
A.1:2:3
B.3:2:1
C.1:1:1
D.6:3:2
参考答案:D
本题解析:
本题难度:简单
3、实验题 (每空1分,共8分)实验室需要配制0.1 mol・L-1 CuSO4溶液480 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、_______ _、________以及等质量的两片滤纸。
(2)计算,应选择下列正确________
A.需要CuSO4 固体8.0g
B.需要CuSO4・5H2O晶体12.0 g
C.需要CuSO4・5H2O晶体12.5 g
D.需要CuSO4固体7.7 g
(3)称量。所用砝码生锈则所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________ 。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了______________________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,
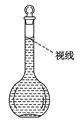
所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
参考答案:(8分,每空1分)
(1)500 mL容量瓶 胶头滴管
本题解析:
试题分析:(1)配制480mL溶液时需要选择500mL的容量瓶,还需要胶头滴管定容;
(2)500mL0.1 mol・L-1 CuSO4溶液中含有硫酸铜的物质的量是0.5L×0.1mol/L=0.05mol,硫酸铜的质量是0.05mol×160g/mol=8.0g,或者选择CuSO4・5H2O晶体,质量是0.05mol×250g/mol=12.5g,所以答案选AC;
(3)所用砝码生锈,称取的溶质的质量偏大,溶质的物质的量偏大,溶液的浓度偏高;
(4)溶解固体物质,用玻璃棒搅拌可以加速固体的溶解;
(5)配制一定物质的量浓度溶液,在移液操作中应该用玻璃棒将溶液引流入容量瓶,并洗涤烧杯2-3次,保证溶质全部转移到容量瓶,防止产生误差;
(8)定容时,仰视刻度线,导致所配溶液的体积偏大,溶液的浓度偏低;
考点:考查一定物质的量浓度溶液的配制过程、仪器以及误差分析
本题难度:一般
4、选择题 NA为阿伏加德罗常数,下列物质所含分子数最少的是
A.标准状况下4.48L氧气
B.11g二氧化碳气体(CO2的摩尔质量是44g・mol-1)
C.0.5mol氨气
D.含NA个氢分子的氢气
参考答案:A
本题解析:
试题分析:将各项数据换算成物质的量,物质的量越小,含有的分子数越少,
A、标准状况下4.48L氧气的物质的量是0.2mol;B、11g二氧化碳气体物质的量是0.25mol;C、0.5mol氨气;D、含NA个氢分子的氢气物质的量为1mol,选A。
考点:考查物质的量的计算。
本题难度:一般
5、选择题 绿色植物是空气天然的“净化器”,研究发现,1亩柳杉每天可以吸收5mol SO2。则1亩柳杉每天吸收的SO2的质量为
A.320g
B.160g
C.64g
D.32g
参考答案:A
本题解析:
试题分析:根据m=n×M=5mol×64g/mol=320g,选A 。
考点:有关物质的量的计算。
本题难度:简单