微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把铝条放入盛有过量的稀盐酸的试管中,不影响氢气产生速率的因素是( )
A.盐酸的浓度
B.铝条的表面积
C.溶液的温度
D.加少量Na2SO4固体
参考答案:D
本题解析:
试题分析:A.盐酸的浓度决定H+浓度的大小,H+浓度不同,反应速率不同,故A不选;B.固体表面积越大,反应速率越快,因此铝条的表面积影响反应速率,B不选;C.反应的温度不同,活化分子的百分数不同,则反应速率不同,故C不选;D.加少量Na2SO4固体,不参与反应,且溶液浓度不变,反应速率不变,故D选;答案选D。
考点:考查化学反应速率的影响因素
本题难度:一般
2、填空题 (14分)碘在科研与生活中有重要应用,某兴趣小组用0.50 mol・L-1 KI、0.2%淀粉溶液、0.20 mol・L-1 K2S2O8、0.10 mol・L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I- 2SO42-+I2(慢) I2+2S2O32-
2SO42-+I2(慢) I2+2S2O32-  2I-+ S4O62-(快)
2I-+ S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-)∶n(S2O82-) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号
| 体积V/mL
|
K2S2O8溶液
| 水
| KI溶液
| Na2S2O3溶液
| 淀粉溶液
|
①
| 10.0
| 0.0
| 4.0
| 4.0
| 2.0
|
②
| 9.0
| 1.0
| 4.0
| 4.0
| 2.0
|
③
| 8.0
| Vx
| 4.0
| 4.0
| 2.0
表中Vx mL,理由是 。
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)
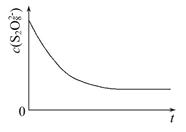
(4)碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为:
2Li(s)+I2(s) 2LiI(s)ΔH 2LiI(s)ΔH
已知:①4Li(s)+O2(g) 2Li2O(s) ΔH1 2Li2O(s) ΔH1
②4LiI(s)+O2(g) 2I2(s)+2Li2O(s)ΔH2 2I2(s)+2Li2O(s)ΔH2
则电池反应的ΔH= ;碘电极作为该电池的 极。
参考答案:(1) Na2S2O3 &
本题解析:
试题分析:(1)根据题目所给信息可知,若溶液中仍存在Na2S2O3,则碘单质将不会存在,溶液不会变蓝色,所以只有将Na2S2O3消耗完时,溶液才会由无色变为蓝色;根据化学方程式,Na2S2O3与K2S2O8完全反应,溶液中不存在碘单质时,Na2S2O3与K2S2O8的物质的量之比为2:1,所以为确保能观察到蓝色,则Na2S2O3的量少些,则n(S2O32-)∶n(S2O82-)<2;
(2)实验①、②中KI溶液、Na2S2O3溶液、淀粉溶液的体积不变,且K2S2O8溶液与水的总体积是10.0mL,该实验的目的是探究反应物浓度对化学反应速率的影响,为保证反应物K2S2O8浓度改变,而其他的条件不变,才能达到实验目的,所以在实验③中K2S2O8溶液与水的总体积必须也是10.0mL,则Vx=2.0mL;
(3)降低温度,该反应的反应速率减慢,而使用催化剂则会加快反应速率,反应完全时溶液中c(S2O82-)不变,所以对应的图像为 ; ;
(4)在2Li(s)+I2(s) 2LiI(s)中I元素的化合价降低,发生还原反应,所以碘作电池的正极,根据盖斯定律可知,ΔH=(①-②)/2=(△H1-△H2)/2. 2LiI(s)中I元素的化合价降低,发生还原反应,所以碘作电池的正极,根据盖斯定律可知,ΔH=(①-②)/2=(△H1-△H2)/2.
考点:考查对实验现象的分析,化学反应速率与图像的关系,盖斯定律的应用
本题难度:困难
3、选择题 下列肯定能使化学反应速率增大的措施是[???? ]
A.增加反应物的量
B.增大压强
C.升高温度
D.使用催化剂
参考答案:C
本题解析:
本题难度:一般
4、选择题 (1)控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察测定因调节变量改变而改变的因素(因变量),从而分析得到研究结论。中学化学中应用控制变量的方法研究问题的例子很多。请分析或设计:
①在研究浓度对化学反应速率的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验(Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O)
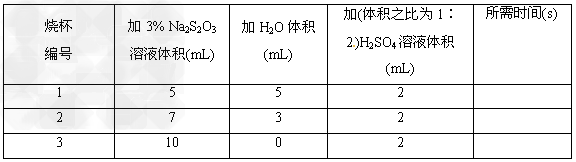
在三个烧杯(底部有黑色“十”字标记)内分别加入表中所示体?积的三种液体,搅拌并开始计时,到出现浑浊使烧杯底部“十”字看不见时停止计时。比较所需时间,得出浓度对化学反应速率影响的结论。实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是____________________,因变量是______________。
②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:____________________________________________________________________________________________________________________。
(2)373?K时,H2PO3-与OH-发生如下反应:H2PO3-+OH- HPO32-+?H2O 反应结果如下表所示 HPO32-+?H2O 反应结果如下表所示
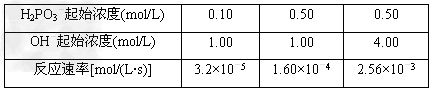
如果用v=kcm(H2PO3-)・cn(OH-)表示反应速率(k为与浓度无关的常数)
①k=________,m=________,n=________。
②若c(H2PO3-)的起始浓度为0.20?mol/L,c(OH-)的起始浓度为1.50?mol/L,则反应速率v=
________。
参考答案:(1)①Na2S2O3溶液的浓度;所需时间;②取三支试管各放
本题解析:
本题难度:一般
5、选择题 硫代硫酸钠与稀盐酸的反应Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O在加热条件下反应速度加快,原因主要是
A.该反应是吸热反应,且可逆,加热使平衡向正向移动
B.加热促使SO2逸出,使平衡向正向移动
C.加热促进S2O32-与H+的碰撞,使反应加速
D.加热促进Na+与Cl-的碰撞,使反应加速
参考答案:C
本题解析:
试题分析:温度升高,反应速率加快的原因是增加了反应微粒的碰撞几率和活化分子的百分含量,C正确。
本题难度:一般
|